Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Ta có phương trình: 2HCl + CaCO3 → CaCl2 + CO2↑ + H2O
=> Khi cho mẩu đá vôi tác dụng với dung dịch HCl thì có khí không màu thoát ra, khí đó là carbon dioxide
- Diện tích bề mặt càng lớn, tốc độ phản ứng càng lớn

- Ta có phương trình: HCl + CaCO3 → CaCl2 + CO2↑ + H2O
=> Khi cho mẩu đá vôi tác dụng với dung dịch HCl thì có khí không màu thoát ra, khí đó là carbon dioxide
- Nồng độ HCl càng cao thì tốc độ phản ứng diễn ra càng nhanh.
- Giải thích: để phản ứng xảy ra, cần phải có sự va chạm giữa HCl và CaCO3. Ở ống nghiệm 2, nồng độ HCl lớn gấp đôi ở ống nghiệm 1, do vậy số va chạm của HCl và CaCO3 (trong cùng 1 đơn vị thời gian) sẽ lớn hơn, từ đó tốc độ phản ứng ở ống nghiệm 2 là lớn hơn

- Ta có phương trình: 2H2O2 → 2H2O + O2↑
=> Dung dịch H2O2 3% ở điều kiện thường phân hủy chậm và có khí không màu thoát ra, khí đó là Oxygen
- Khi có chất xúc tác, khí thoát ra nhiều hơn
=> Chất xúc tác MnO2 làm tăng tốc độ phân hủy H2O2

C
Hiện tượng: đồng tan cho dung dịch màu xanh, có bọt khí thoát ra không màu.
C u + 2 H 2 S O 4 đ ặ c → t ° C u S O 4 ( x a n h ) + S O 2 ( ↑ k h ô n g m à u ) + 2 H 2 O

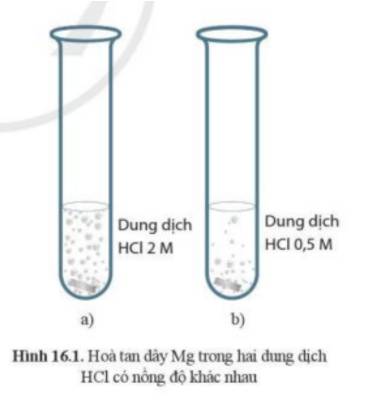
- Ở ống nghiệm (a) có hiện tượng sủi bọt khí nhiều hơn
=> Phản ứng ở ống nghiệm (a) xảy ra mãnh liệt hơn
=> Dây Mg ở ống nghiệm (a) sẽ bị tan hết trước
Mg + 2HCl → MgCl2 + H2↑

1. Sự thay đổi màu sắc trong ống nghiệm được đung nóng nhanh hơn.
2. Khi nhiệt độ tăng, tốc độ phản ứng sẽ tăng lên

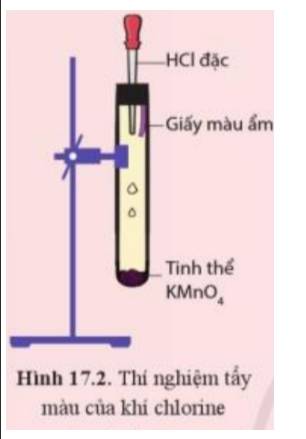
- Hiện tượng: Xuất hiện khí màu vàng và giấy màu ẩm bị nhạt màu dần rồi mất màu
- Giải thích:
+ Khi nhỏ HCl đặc vào tinh thể KMnO4, sản phẩm tạo thành có khí chlorine:
2KMnO4 + 16HCl → 2MnCl2 + 2KCl + 5Cl2 + 8H2O
+ Khí chlorine tác dụng với nước ở giấy màu ẩm tạo thành hỗn hợp có tính tẩy màu: HCl và HClO
Cl2(aq) + H2O(l) \( \rightleftharpoons \) HCl(aq) + HClO(aq)
=> Dung dịch này còn được gọi là dung dịch nước chlorine, có tính tẩy màu, sát khuẩn

Chọn B
Ở nhiệt độ t 2 hỗn hợp khí có tỉ khối hơi so với H 2 lớn hơn nhiệt độ t 1 → ở nhiệt độ t 2 có lượng N 2 O 4 lớn hơn ở nhiệt độ t 1 .
Mà t 1 > t 2 → khi giảm nhiệt độ cân bằng chuyển dịch theo chiều thuận (tạo thành N 2 O 4 không màu); khi tăng nhiệt độ cân bằng chuyển dịch theo chiều nghịch (tạo thành N O 2 màu nâu).
- Ta có phương trình: 2HCl + Fe → FeCl2 + H2↑
=> Khi cho đinh sắt tác dụng với dung dịch HCl thì có khí không màu thoát ra, khí đó là hydrogen
- Nhiệt độ càng cao, tốc độ phản ứng càng lớn