Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 3 :
\(n_{MgO}=\dfrac{8}{40}=0,2\left(mol\right)\)
1) Pt : \(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,2 0,4 0,2
\(n_{MgCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{MgCl2}=0,2.136=27,2\left(g\right)\)
2) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
\(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(m_{ddHCl}=\dfrac{14,6.100}{20}=73\left(g\right)\)
Chúc bạn học tốt
Mình xin lỗi bạn nhé , bạn sửa lại giúp mình chỗ :
\(m_{MgCl2}=0,2.95=19\left(g\right)\)

a) Mg + 2HCl → MgCl2 + H2
b) nMg =\(\dfrac{14,4}{24}\)=0,6 mol => nH2 = nMg= 0,6 mol <=> V H2 = 0,6.22,4 = 13,44 lít
c) nHCl = 2nMg = 1,2mol => mHCl = 1,2.36,5 = 43,8 gam
=> C%HCl = \(\dfrac{43,8}{200}.100\) =21,9%

Ta có: \(n_{ZnO}=\dfrac{16,2}{81}=0,2\left(mol\right)\)
a, PT: \(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
______0,2_____0,4____0,2 (mol)
b, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\Rightarrow m_{ddHCl}=\dfrac{14,6}{10\%}=146\left(g\right)\)
c, \(C\%_{ZnCl_2}=\dfrac{0,2.136}{16,2+146}.100\%\approx16,77\%\)
Bạn tham khảo nhé!

\(a/\\MgO+2HCl \to MgCl_2+H_2O\\ n_{MgO}=\frac{8}{40}=0,2(mol)\\ b/\\ n_{HCl}=0,2.2=0,4(mol)\\ CM_{HCl}=\frac{0,4}{0,2}=2M\)

nH2 = \(\frac{1,68}{22,4}\) = 0,075 (mol)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2\(\uparrow\) (1)
0,075 <--------0,075 <--0,075 (mol)
MgO + 2HCl \(\rightarrow\) MgCl2 + H2O (2)
%mMg= \(\frac{0,075.24}{5,8}\) . 100% = 31,03 %
%m MgO = 68,97%
nMgO = \(\frac{5,8-0,075.24}{40}\) = 0,1 (mol)
Theo pt(2) nMgCl2 = nMgO= 0,1 (mol)
mdd sau pư = 5,8 + 194,35 - 0,075.2 = 200 (g)
C%(MgCl2) = \(\frac{95\left(0,075+0,1\right)}{200}\) . 100% = 8,3125%

nH2SO4=2.0,2=0,4mol
PTHH: 2NaOH+H2SO4=> Na2SO4+2H2O
0,8mol<-0,4mol->0,4mol->0,8mol
theo định luật btoan khói lượng mdd Na2SO4
= mNaOH+mH2SO4-mH2O=0,8.40+1,3.0,4.-0,8.18=56,6g
mNa2SO4=04.142=56,8
=> C%=32,25%
Bài 1: PTHH: 2NaOH + H2SO4 --> Na2SO4 + 2H2O
Đổi: 200 ml = 0,2 lít
Số mol của H2SO4 là: 0,2 . 2 = 0,4 mol
Khối lượng dung dịch axit là: 200 . 1,3 = 260 gam
Khối lượng của NaOH là: 0,4 . 2 . 40 = 32 gam
Khối lượng dung dịch sau phản ứng là: 260 + 32 = 292 gam
Khối lượng Na2SO4 là: 0,4 . 142 = 56,8 gam
Nồng độ phần trăm Na2SO4 có trong dung dịch sau phản ứng là: ( 56,8 : 292 ) . 100% = 19,5%

a)Zn +2HCl------>ZnCl2 +H2
\(b.\)Ta có
n\(_{Zn}=\frac{6.6}{65}=0,1mol\)
Theo Pthh
n\(_{HCl}=2n_{Zn}=0,2mol\)
C\(_M\left(HCl\right)=\frac{0,1}{0,1}=0,5\left(M\right)\)
c) Tính nồng độ mol của dd sau pư nha bạn...Bài này ko đủ dữ kiện để tính nồng độ phần tram
Theo pthh
n\(_{Z_{ }nCl2}=n_{Zn}=0,1mol\)
C\(_{M\left(ZnCl2\right)}=\frac{0,1}{0,1}=1\left(M\right)\)
d) Theo pthh
n\(_{H2}=n_{Zn}=0,1mol\)
V\(_{H2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\)
Chúc bạn học tốt
Nhớ tích cho mình nhé

a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
nFe = nH2 = 0,3 (mol)
\(\Rightarrow m_{Fe}=0,3.56=16,8\left(g\right)\)
b) nHCl = 2.nH2 = 0,6 (mol)
\(\Rightarrow V_{ddHCl}=\dfrac{0,6}{0,3}=2\left(l\right)\)
c) \(n_{FeCl_2}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow C_{M\left(FeCl_2\right)}=\dfrac{0,3}{2}=0,15M\)
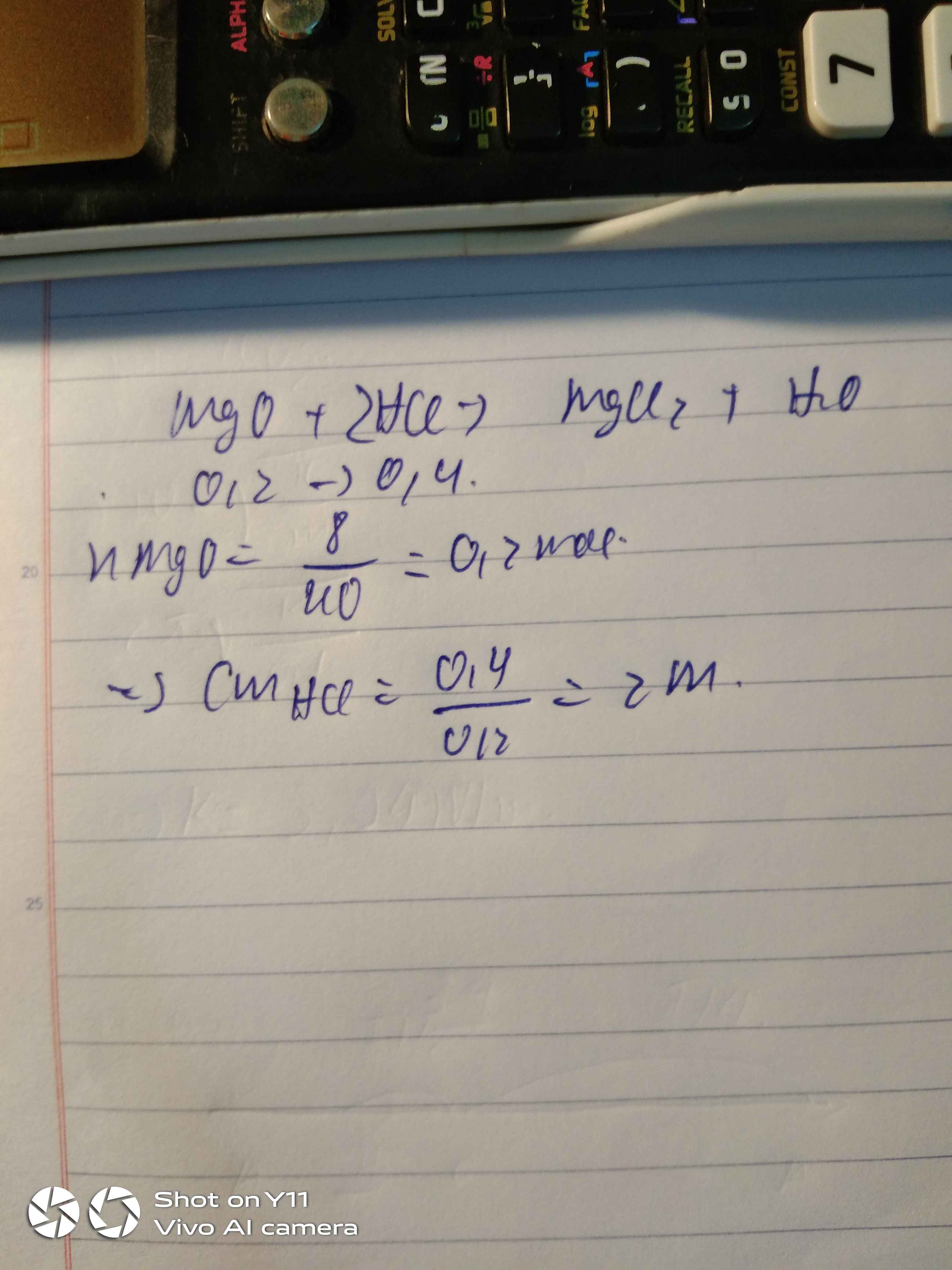
nMgO = 8/40=0,2(mol)
a) PTHH: MgO +2 HCl -> MgCl2 + H2O
0,2________0,4________0,2(mol)
b) mHCl= 0,4.36,5=14,6(g)
=>C%ddHCl= (14,6/146).100=10%
c) mddMgCl2= 8+ 146= 154(g)
mMgCl2= 0,2.95=19(g)
=>C%ddMgCl2= (19/154).100=12,338%
số mol của magie oxit
nMgO = \(\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{8}{40}=0,2\left(mol\right)\)
a) MgO + 2HCl → MgCl2 + H2O\(|\)
1 2 1 1
0,2 0,4 0,2
b) Số mol của axit clohidric
nHCl = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
Khối lượng của axit clohidric
mHCl = nHCl . MHCl
= 0,4. 36,5
= 14,6 (g)
Nồng độ phần trăm của dung dịch axit clohidric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{14,6.100}{146}=10\)0/0
c) Số mol của magie clorua
nMgCl2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Khối lượng của magie clorua
mMgCl2 = nMgCl2 . MMgCl2
= 0,2. 95
= 19 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mMgO + mHCl
= 8 + 146
= 154 (g)
Nồng độ phần trăm của magie clorua
C0/0MgCl2 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{19.100}{154}=12,34\)0/0
Chúc bạn học tốt