Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt công thức 2 oxit là \(\begin{matrix}A_2O_3&x\left(mol\right)\\BO&x\left(mol\right)\end{matrix}\)
\(\begin{matrix}A_2O_3&+6HCl&\rightarrow&2ACl_3&+3H_2O&\\x&6x&&2x&3x&\left(mol\right)\\BO&+2HCl&\rightarrow&BCl_2&+H_2O&\\x&2x&&x&x&\left(mol\right)\end{matrix}\)
Theo đề ta có: nHCl=8x=0,8 (mol) ⇒x=0,1(mol)
Khối lượng hỗn hợp: 0,1(2MA+48)+0,1(MB+16)=18,2
⇒2MA+MB=118 ⇒\(\overline{M}_{A,B}=\dfrac{118}{3}\approx39,333\left(g/mol\right)\)
Nghĩa là hoặc MA≤39 hoặc MB≤39 và điều kiện MB chẵn vì \(M_A=\dfrac{118-M_B}{2}\)để MA nguyên
-TH1: MA≤39 Mà A có hóa trị III ⇒ A là Al ⇒MB=64 ⇒B là Cu (Thõa điều kiện B hóa trị II, MB nguyên)(Nhận)
-TH2: MB≤39 mà B có hóa trị II ⇒ B là Mg ⇒MA=47⇒ Loại vì không có A thõa)
Vậy 2 oxit kim loại đó là Al2O3 và CuO
Khi cô cạn X ta thu được 2 muối là \(\begin{matrix}AlCl_3&0,2\left(mol\right)\\CuCl_2&0,1\left(mol\right)\end{matrix}\)
m=0,2.133,5+0,1.135=40,2(g)

a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
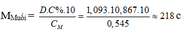
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
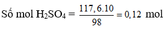
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%

Phương trình hóa học của phản ứng:
Cu + H 2 SO 4 → Không phản ứng
Fe + H 2 SO 4 → FeSO 4 + H 2
n H 2 = 2,24/22,4 = 0,1 mol
n Fe = 0,1 x 56 = 5,6g. Khối lượng Cu không hòa tan là
m = 10 - 5,6 = 4,4g

\(Fe_2O_3\left(0,12\right)+H_2\underrightarrow{t^o}2Fe\left(0,24\right)+3H_2O\)
.........\(MO+H_2\underrightarrow{t^o}M+H_2O\) (1)
___MM + 16(g)__MM
_____12g_______9,6(g)
hh chất rắn A: \(Fe_2O_3\) dư, MO dư, Fe , M
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(MO+H_2SO_4\rightarrow MSO_4+H_2O\)
\(Fe\left(0,24\right)+H_2SO_4\rightarrow FeSO_4+H_2\left(0,24\right)\)
Chất rắn Z: M
\(n_{H_2}=\dfrac{5,376}{22,4}=0,24\left(mol\right)\)
\(m_{Fe_2O_3}=0,12.160=19,2\left(g\right)\)
\(\Rightarrow m_{MO}=31,2-19,2=12\left(g\right)\)
Từ PTHH(1) có: \(9,6M_M+153,6=12M_M\)
\(\Rightarrow2,4M_M=153,6\Rightarrow M_M=64\)
=> M là Cu.

nH2=13,14:22,4=0,6 mol
PTHH: 2Al+6HCl=>2Al2Cl3+3H2
0,4<-1,2<----0,4<-----0,6
=> Al=0,4.27=10,8g
CMHCL=1,2:0,4=3M
CM Al2Cl3=0,4:0,4=1M
bài 2: nH2=0,2mol
PTHH: 2A+xH2SO4=> A2(SO4)x+xH2
0,4:x<---------------------------0,2
ta có PT: \(\frac{13}{A}=\frac{0,4}{x}\)<=> 13x=0,4A
=> A=32,5x
ta lập bảng xét
x=1=> A=32,5 loiaj
x=2=> A=65 nhận
x=3=> A=97,5 loại
=> A là kẽm (Zn)

R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)



Em làm được rồi ạ