Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nH2= 1,344 / 22,4=0,06 mol
Khoi luong Fe va Al la 2,52 - 0,3= 2,22 g
Fe + 2HCl --> FeCl2 + H2
x mol 2xmol x mol
2Al + 6HCl --> 2AlCl3 + 3H2
y mol 3ymol 3/2 mol
56x + 27y = 2,22 (1)
x + 3/2y = 0,06 (2)
Tu (1) va (2) ta duoc => x= 0,03
=> y=0,02
a/ mFe=0,03.56=1,68g
mAl=0,02.27=0,54g
%mCu=(0,3/2,52).100=11,9%
%mFe=(1,68/2,52).100=66,6%
%mAl=21,5%
b/ mct=0,12.36,5=4,38g
%CHCl= (4,38/200).100=2,19%

\(a) m_{Cu} = 9,6(gam)\\ n_{Al} = a(mol) ; n_{Fe} = b(mol)\\ \Rightarrow 27a + 56b = 16,55 -9,6 =6,95(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{3,92}{22,4} = 0,175(2)\\ (1)(2) \Rightarrow a = 0,05 ; b = 0,1\\ m_{Al} = 0,05.27 = 1,35(gam); n_{Fe} = 0,1.56 = 5,6(gam)\)
\(b) n_{HCl} = 2n_{H_2} = 0,175.2 = 0,35(mol) \Rightarrow m_{HCl} = 0,35.36,5 = 12,775(gam)\)

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,1<-------------------------0,15
=> \(\%m_{Al}=\dfrac{0,1.27}{9,1}.100\%=29,67\%=>\%m_{Cu}=100\%-29,67\%=70,33\%\)

BT2:
Gọi công thức hóa học của oxit kim loại M và hóa trị của M trong phản ứng với axit là MxOy, a
ta có phương trình:
MxOy + yH2 -------------> yH2O + xM (1)
2M+2aHCl-------> 2MCla + aH2 (2)
Số mol H2(phản ứng 1)
=0,045(mol)
nM(phản ứng 2) =\(\dfrac{0,045}{a}\)
theo đè bài thì số mol của M ở phản ứng 1 và phản ứng 2 là như nhau
<=> \(\dfrac{0,06x}{y}=\dfrac{0.045}{a}\)
và ta lại có khối lượng của oxit là 3,48g
=> \(\dfrac{0,06x}{y}.\left(Mx+16y\right)=34,8\)
=> \(\dfrac{0,06x.Mx}{y}=2,52\)
=> M= 28a
lập bảng ta có: M là Fe
MFexOy= \(\dfrac{3.48y}{0,06}=56x+16y\)
=> \(3,48y=3,36x+0,96y\)
=> \(2,52y=3,36x\)
=> \(\dfrac{x}{y}=\dfrac{2,52}{3,36}=\dfrac{3}{4}\)
\(CTHH:Fe_{3_{ }}O_4\)

Đặt \(\left\{{}\begin{matrix}n_{Al}=x\\n_{Zn}=y\\n_{Cu}=z\end{matrix}\right.\) ( mol )
\(m_{hh}=27x+65y+64z=22,8\left(g\right)\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
x 1,5x ( mol )
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
y y ( mol )
\(n_{H_2}=1,5x+y=\dfrac{11,2}{22,4}=0,5\left(mol\right)\) (2)
B là Cu
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
z z ( mol )
\(n_{CuO}=z=\dfrac{5,5}{80}=0,06875\left(mol\right)\) (3)
\(\left(1\right);\left(2\right);\left(3\right)\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,2\\z=0,06875\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Zn}=0,2.65=13\left(g\right)\\m_{Cu}=22,8-5,4-13=4,4\left(g\right)\end{matrix}\right.\)

Phần 1 :
$m_{Cu} = 0,4(gam)$
Gọi $n_{Fe} = a ; n_{Al} = b \Rightarrow 56a + 27b + 0,4 = 1,5 : 2 = 0,75(1)$
$Fe + 2HCl \to FeCl_2 + H_2$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$n_{H_2} = a + 1,5b = \dfrac{896}{1000.22,4} = 0,04(2)$
Từ (1)(2) suy ra a = -0,025 < 0$
$\to$ Sai đề

\(n_{Al} = a\ ; n_{Fe} =b\\ \Rightarrow 27a + 56b = 11(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{8,96}{22,4} = 0,4(2)\\ (1)(2) \Rightarrow a = 0,2 ; b = 0,1\\ n_{HCl\ dư} = \dfrac{200.21,9\%}{36,5} - 0,2.3 - 0,1.2 = 0,4(mol)\\ m_{dd\ sau\ pư} = 11 + 200 - 0,4.2 = 210,2(gam)\\ C\%_{HCl} = \dfrac{0,4.36,5}{210,2}.100\% = 6,95\%\\ \)
\(C\%_{AlCl_3} = \dfrac{0,2.133,5}{210,2}.100\% = 12,7\%\\ C\%_{FeCl_2} = \dfrac{0,1.127}{210,2}.100\% = 6,04\%\)

a)
\(n_{H_2\left(1\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2 (1)
0,6<----------------------0,3
=> mNa = 0,6.23 = 13,8 (g)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1<-0,2
=> mFe = 0,1.56 = 5,6 (g)
mCu = 10 (g)
\(\left\{{}\begin{matrix}\%Na=\dfrac{13,8}{13,8+5,6+10}.100\%=46,94\%\\\%Fe=\dfrac{5,6}{13,8+5,6+10}.100\%=19,05\%\\\%Cu=\dfrac{10}{13,8+5,6+10}.100\%=34,01\%\end{matrix}\right.\)
b)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,3}{y}\)<--0,3
=> \(M_{Fe_xO_y}=\dfrac{17,4}{\dfrac{0,3}{y}}=58y\left(g/mol\right)\)
=> 56x = 42y
=> \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
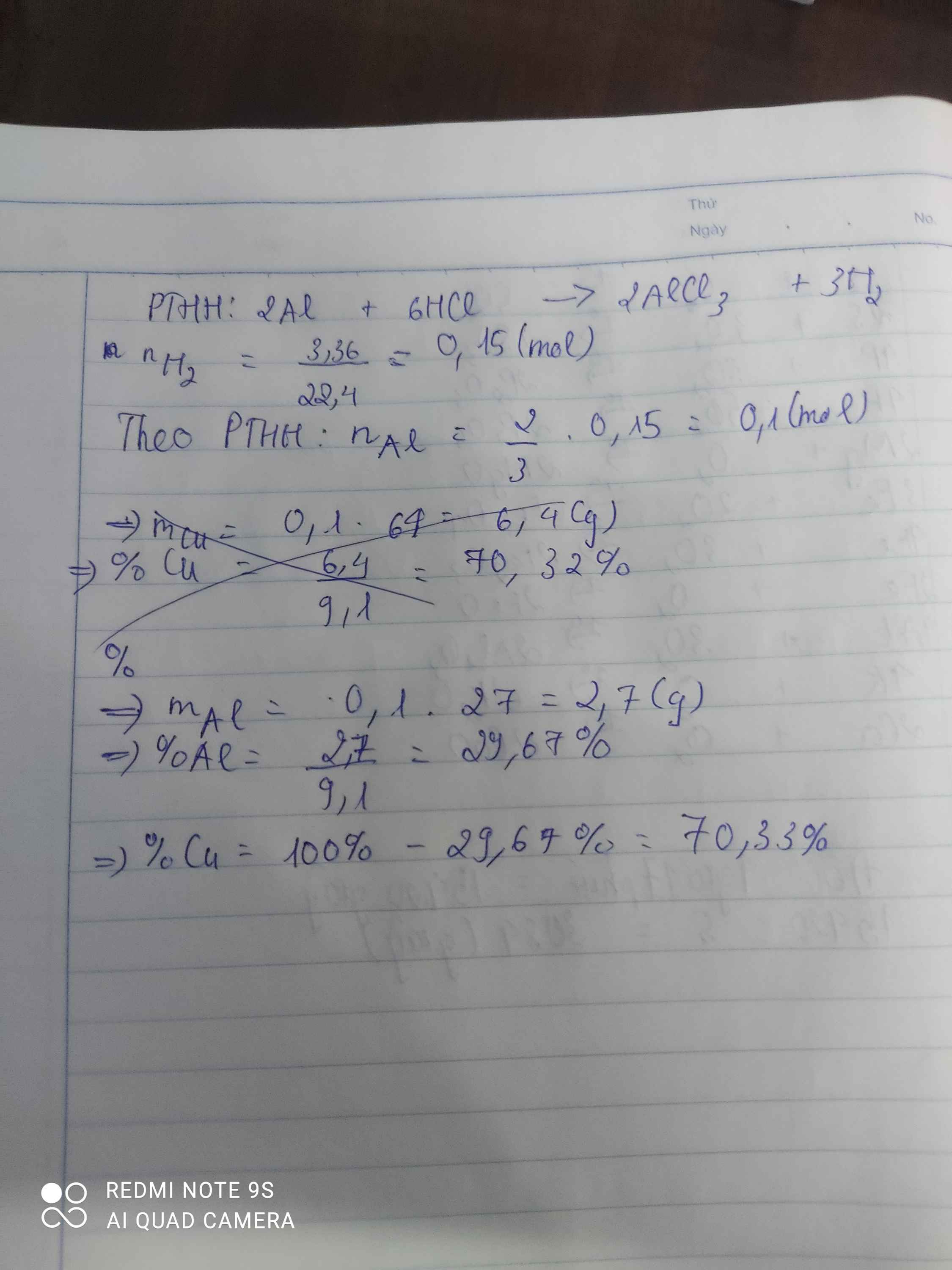
Bài làm:
nH2= 1,344 / 22,4=0,06 mol
Khối lượng Fe và Al là: 2,52 ‐ 0,3= 2,22 g
Fe + 2HCl ‐‐> FeCl2 + H2
x mol 2xmol x mol
2Al + 6HCl ‐‐> 2AlCl3 + 3H2
y mol 3ymol 3/2 mol
56x + 27y = 2,22 ﴾1﴿
x + 3/2y = 0,06 ﴾2﴿
Từ﴾1﴿ và ﴾2﴿ ta có => x= 0,03
=> y=0,02
a/ mFe=0,03.56=1,68g
mAl=0,02.27=0,54g
%mCu=﴾0,3/2,52﴿.100=11,9%
%mFe=﴾1,68/2,52﴿.100=66,6%
%mAl=21,5%
b/ m\(_{ct}\) =0,12.36,5=4,38g
%C \(_{hcl}\)= ﴾4,38/200﴿.100=2,19%