Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Cu không tác dụng được với dd H2SO4 loãng.
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{Zn}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow\%m_{Zn}=\dfrac{0,1.65}{10,5}.100\approx61,905\%\\ \Rightarrow\%m_{Cu}\approx38,095\%\)
anh giúp em bài này với https://hoc24.vn/cau-hoi/giup-minh-voi-trong-tam-giai-thich-ki-cai-de-nha-cam-on.2017646398420

Chọn B
Chỉ có Zn phản ứng với H 2 S O 4 , Cu không phản ứng


a. PTHH:
\(Zn+H_2SO_4--->ZnSO_4+H_2\)
\(Cu+H_2SO_4--\times-->\)
b. Theo PT: \(n_{Zn}=n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow m_{_{ }Zn}=0,1.65=6,5\left(g\right)\)
\(\Rightarrow\%_{m_{Zn}}=\dfrac{6,5}{10,5}.100\%=61,9\%\)
\(\%_{m_{Cu}}=100\%-61,9\%=31,8\%\)
\(Zn + H_2SO_4 \rightarrow ZnSO_4 + H_2\)
Cu không phản ứng H2SO4 loãng nhé
\(n_{H_2}= \dfrac{2,24}{22,4}= 0,1 mol\)
Theo PTHH:
\(n_{Zn}=n_{H_2}= 0,1 mol\)
\(\Rightarrow m_{Zn}= 0,1 . 65= 6,5 g\)
\(\Rightarrow\)%mZn=\(\dfrac{6,5}{10,5} . 100\)%~ 61,9%
\(\Rightarrow\)%mCu= 100% - 61,9%=38,1 %

\(a.Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ b.n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{Zn}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow\%m_{Zn}=\dfrac{0,1.65}{10,5}.100=61,9\%\\ \%m_{Cu}=100-61,9=38,1\%\)

$Zn + H_2SO_4 \to ZnSO_4 + H_2$
Theo PTHH :
$n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$\%m_{Zn} = \dfrac{0,1.65}{10,5}.100\% = 61,9\%$
Chọn đáp án A

Zn+ H2SO4→ ZnSO4+ H2↑
(mol) 0,1 0,1 0,1
a)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\left(lít\right)\)
→mZn=n.M=0,1.65= 6,5(g)
→mCu= 10- 6,5= 3,5(g)
=> \(\%m_{Zn}=\dfrac{6,5}{10}.100\%=65\%\)
\(\%m_{Cu}=100\%-65\%=35\%\)
b) \(C_{M_{H_2SO_4}}=\dfrac{n}{V}=\dfrac{0,1}{0,1}=1M\)

a) \(Zn + H_2SO_4 \rightarrow ZnSO_4 + H_2\)
Cu không pư H2SO4 loãng
b)
\(n_{H_2}=\dfrac{2,24}{22,4}= 0,1 mol\)
Theo PTHH:
\(n_{Zn}= n_{H_2}= 0,1 mol\)
\(\Rightarrow m_{Zn}= 0,1 . 65= 6,5 g\)
\(\Rightarrow m_{Cu}= m_{hh KL} - m_{Zn}= 10 - 6,5 = 3,5 g\)
Gọi \(n_{Cu}=x\left(mol\right)\)\(;n_{Zn}=y\left(mol\right)\)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,1
\(m_{Zn}=0,1\cdot65=6,5g\)
\(m_{Cu}=10-6,4=3,6g\)
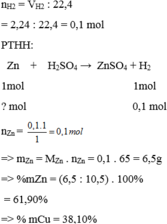
Cu ko tác dụng được với H2SO4 loãng
=> khí H2 sinh ra là do Zn tác dụng hết với H2SO4
\(Zn+H_2SO_4->ZnSO_4+H_2\)
0.2.......................................0,2
n H2 = 4,48 : 22,4 = 0,2 mol
m Zn = 0,2 . 65 =13 g
m Cu = 25 - 13 =12 g