Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Pt : Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
1 3 1 3
0,03 0,1 0,03
b) Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
Số mol của nhôm sunfat
nAl2(SO4)3 = \(\dfrac{0,1.1}{3}=0,03\left(mol\right)\)
Khối lượng của nhôm sunfat
mAl2(SO4)3 = nAl2(SO4)3 . MAl2(SO4)3
= 0,03 . 342
= 10,26 (g)
c) Số mol của nhôm oxit
nAl2O3 = \(\dfrac{0,1.1}{3}=0,03\left(mol\right)\)
Khối lượng của nhôm oxit
mAl2O3 = nAl2O3 . MAl2O3
= 0,03 . 102
= 3,06 (g)
Chúc bạn học tốt

Gọi số mol của Al2O3, Fe2O3 là 2a, 3a (mol)
PTHH: Al2O3 + 3H2SO4 --> Al2(SO4)3 + 3H2O
2a---->6a
Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
3a----->9a
=> 6a + 9a = 0,3
=> a = 0,02
=> \(\left\{{}\begin{matrix}n_{Al_2O_3}=0,04\left(mol\right)\\n_{Fe_2O_3}=0,06\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Al_2O_3}=\dfrac{0,04.102}{0,04.102+0,06.160}.100\%=29,825\%\\\%m_{Fe_2O_3}=\dfrac{0,06.160}{0,04.102+0,06.160}.100\%=70,175\%\end{matrix}\right.\)

\(n_{Al2O3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
Pt : \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O|\)
1 3 1 3
0,2 0,6 0,2
\(n_{H2SO4}=\dfrac{0,2.3}{1}=0,6\left(mol\right)\)
⇒ \(m_{H2SO4}=0,6.98=58,8\left(g\right)\)
\(n_{Al2\left(SO4\right)3}=\dfrac{0,6.1}{3}=0,2\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=0,2.342=68,4\left(g\right)\)
Chúc bạn học tốt

Phương trình hóa học của phản ứng:
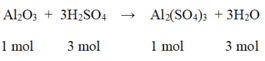
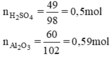
So sánh tỉ lệ 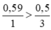 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
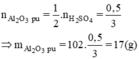
mAl2O3 (dư) = 60 - 17 = 43(g)

PTHH: \(2Al\left(OH\right)_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+6H_2O\)
Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{7,8}{78}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2SO_4}=0,15mol\\n_{Al_2\left(SO_4\right)_3}=0,05mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{H_2SO_4}=0,15\cdot98=14,7\left(g\right)\\m_{Al_2\left(SO_4\right)_3}=0,05\cdot342=17,1\left(g\right)\end{matrix}\right.\)

\(n_{Al_2O_3}=\dfrac{20,4}{102}=0,2mol\)
\(n_{H_2SO_4}=\dfrac{78,84}{98}=0,8mol\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
0,2 < 0,8 ( mol )
0,2 0,6 0,2 0,6 ( mol )
\(m_{H_2SO_4\left(dư\right)}=\left(0,8-0,6\right).98=19,6g\)
Cách 1:\(m_{Al_2\left(SO_4\right)_3}=0,2.342=68,4g\)
Cách 2:
\(m_{H_2SO_4}=0,6.98=58,8g\)
\(m_{H_2O}=0,6.18=10,8g\)
Áp dụng ĐL BTKL, ta có:
\(m_{Al_2O_3}+m_{H_2SO_4}=m_{Al_2\left(SO_4\right)_3}+m_{H_2O}\)
\(\rightarrow m_{Al_2\left(SO_4\right)_3}=20,4+58,8-10,8=68,4g\)
nAl2O3=20,4102=0,2molnAl2O3=20,4102=0,2mol
nH2SO4=78,8498=0,8molnH2SO4=78,8498=0,8mol
Al2O3+3H2SO4→Al2(SO4)3+3H2OAl2O3+3H2SO4→Al2(SO4)3+3H2O
0,2 < 0,8 ( mol )
0,2 0,6 0,2 0,6 ( mol )
mH2SO4(dư)=(0,8−0,6).98=19,6

n H2SO4=\(\dfrac{10\%.490}{2+32+16.4}=0,5mol\)
n Al2O3 =\(\dfrac{10,2}{27.2+16.3}=0,1mol\)
\(Al_2O_3+3H_2SO_4->Al_2\left(SO_4\right)_3+3H_2O\)
bđ 0,1............0,5
pư 0,1............0,3..................0,1
spu 0 ................0,2................0,1
=> sau pư gồm H2SO4 dư , Al2(S04)3 và H2O
m H2SO4 dư = \(0,2.\left(2+32+16.3\right)=19,6g\)
m Al2(SO4)3 = \(0,1\left(27.2+32.3+16.4.3\right)=34,2g\)
m dd = \(490+10,2=500,2g\)
% Al2(SO4)3 = \(\dfrac{34,2}{500,2}.100\sim6,84\%\)
% H2SO4 dư = \(\dfrac{19,6}{500,2}.100\sim3,92\%\)
nAl2O3=15,3/102=0,15mol
nH2SO4=22,54/98=0,23mol
PTHH:Al2O3+3H2SO4->Al2(SO4)3+3H2O
TheoPT:1mol 3mol 1mol
Theo bài:0,15mol 0,23mol
PỨ: 0,076mol 0,23mol 0,076mol
Còn: 0,074mol 0 0,076mol
Tỉ lệ:\(\dfrac{0,15}{1}>\dfrac{0,23}{3}\)->H2SO4 hết Al2O3 dư tính theo H2SO4
mAl2(SO4)3=0,076.342=25,992g
Nhầm đề f k bn