Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

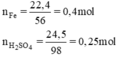
Phương trình hóa học của phản ứng:

So sánh tỉ lệ 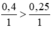 ⇒ Fe dư
⇒ Fe dư
Theo PT nFe (pư) = nH2SO4 = 0,25 mol ⇒ nFe dư = 0,4 – 0,25 = 0,15 mol
mFe dư = 0,15. 56 = 8,4g.
Do khối lượng Fe dư nên tính thể tích khí H2 theo số mol H2SO4.
nH2 = nH2SO4 = 0,25 mol
Vkhí = 0,25 . 22,4 = 5,6l.

\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_{HCl}=\dfrac{m}{M}=\dfrac{18,25}{1+35,5}=0,5\left(mol\right)\\ PTHH:Fe+2HCl->FeCl_2+H_2\)
tỉ lệ 1 : 2 : 1 : 1
n(mol) 0,2------->0,4--------->0,2---->0,2
\(\dfrac{n_{Fe}}{1}< \dfrac{n_{HCl}}{2}\left(\dfrac{0,2}{1}< \dfrac{0,5}{2}\right)\)
`=> Fe` hết, `HCl` dư, tính theo `Fe`
\(n_{HCl\left(dư\right)}=0,5-0,4=0,1\left(mol\right)\\ m_{HCl\left(dư\right)}=n\cdot M=0,1\cdot\left(1+35,5\right)=3,65\left(g\right)\\ V_{H_2\left(dktc\right)}=n\cdot22,4=0,2\cdot22,4=4,48\left(l\right)\)
a) Ta có : PTHH : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có : \(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{m}{M}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
Theo PTHH thì ta có : \(2n_{Fe}=n_{HCl}\)
Giả sử HCl dùng hết : \(\Rightarrow n_{Fe}\) cần dùng là : \(0,25\left(mol\right)\) không thỏa mãn
\(\Rightarrow Fe\) dùng hết ; HCl dư
Số mol HCl dư là :
\(0,5-0,2.2=0,1\left(mol\right)\)
Khối lượng dư của HCl là :
\(0,1.36,5=3,65\left(g\right)\)
b) Do Fe dùng hết nên ta tính H theo Fe
Theo PTHH : \(n_{Fe}=n_{H_2}\)
\(\Rightarrow n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

a) nFe=0,4(mol); nH2SO4=0,5(mol)
PTHH: Fe + H2SO4 -> FeSO4 + H2
Ta có: 0,4/1 < 0,5/1
=> Fe hết, H2SO4 dư. tính theo nFe.
=> nH2= nH2SO4(p.ứ)=nFe=0,4(mol)
=>nH2SO4(dư)=0,5-0,4=0,1(mol)
=>H2SO4(dư)=0,1.98=9,8(g)
b) V(H2,dktc)=0,4.22,4=8,96(l)

\( n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(n_{H_2SO_4}=\dfrac{24,5}{98}=0,25mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1 0,25 0 0
0,1 0,15 0,05 0,15
0 0,1 0,05 0,15
Chất \(H_2SO_4\) dư và dư \(m=0,1\cdot98=9,8g\)
\(V_{H_2}=0,15\cdot22,4=3,36l\)
\(nAl=\dfrac{2,7}{27}=0,1\left(mol\right)\)
\(nH_2SO_4=\dfrac{24,5}{98}=0,25\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
0,1---->0,15------>0,05--------------->0,15
Xét tỉ lệ : \(\dfrac{0,1}{2}< \dfrac{0,25}{3}\)
=> H2SO4 dư vs pứ
\(nH_2SO_{4\left(dư\right)}=0,25-0,15=0,1\left(mol\right)\)
\(mH_2SO_4=\)\(0,1.98=9,8\left(g\right)\)
\(VH_2=0,15.22,4=3,36\left(lít\right)\)

\(n_{Mg}=\dfrac{2.4}{24}=0.1\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.1....................................0.1\)
\(V_{H_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(2H_2+O_2\underrightarrow{^{t^0}}2H_2O\)
\(0.1.....0.05\)
\(m_{O_2\left(dư\right)}=\left(0.5-0.05\right)\cdot32=14.4\left(g\right)\)

a, \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,25}{1}\), ta được Fe dư.
Theo PT: \(n_{Fe\left(pư\right)}=n_{H_2SO_4}=0,25\left(mol\right)\Rightarrow n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(\Rightarrow m_{Fe\left(dư\right)}=0,15.56=8,4\left(g\right)\)
b, \(n_{H_2}=n_{H_2SO_4}=0,25\left(mol\right)\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)

a. PTHH :Fe + H2SO4 -> FeSO4 +H2
nFe = 22,4 : 56 = 0,4 (mol)
nH2SO4 = 24,5 : 98 = 0,25 (mol)
Ta có nFe > nH2SO4 (0,4>0,25) nên Fe dư
nFe dư = 0,4-0,25 = 0,15 (mol)
Vậy mFe dư = 0,15 . 56 = 8,4 (gam)
b, Theo PTHH ta có nH2 = nH2SO4 =0,25 (mol)
=> VH2 thu được (đktc) =0,25 . 22,4 =5,6(lit)
Ta có: \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\ n_{H_2SO_4\left(loãng\right)}=\dfrac{24,5}{98}=0,25\left(mol\right)\)
PTHH: Fe + H2SO4 (loãng) -> FeSO4 + H2\(\uparrow\)
Theo PTHH và đề bài, ta có:
\(\dfrac{n_{Fe\left(đềbài\right)}}{n_{Fe\left(PTHH\right)}}=\dfrac{0,4}{1}>\dfrac{n_{H_2SO_4\left(loãng,đềbài\right)}}{n_{H_2SO_4\left(loãng,PTHH\right)}}=\dfrac{0,25}{1}\)
=> H2SO4 loãng hết, Fe dư nên tính theo \(n_{H_2SO_4\left(loãng\right)}\)
Theo PTHH và đề bài, ta có:
\(n_{H_2}=n_{Fe\left(phảnứng\right)}=n_{H_2SO_4\left(loãng\right)}=0,25\left(mol\right)\\ =>n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
a) Khối lượng Fe dư:
\(m_{Fe\left(dư\right)}=0,15.56=8,4\left(g\right)\)
b) Thể tích khí H2 thu được (ở đktc):
\(V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)

a, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,2}{2}\), ta được Fe dư.
Theo PT: \(n_{Fe\left(pư\right)}=\dfrac{1}{2}n_{HCl}=0,1\left(mol\right)\Rightarrow n_{Fe\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe\left(dư\right)}=0,1.56=5,6\left(g\right)\)
b, \(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Thank ♥️♥️♥️♥️