Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
Khối lượng CaO: 
Số mol CaO:
Pt:
 số mol Ca (OH)2
số mol Ca (OH)2
Vậy khối lượng Ca(OH)2tạo thành: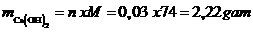
Vậy mct = 2,22 gam
 Mà
Mà 
Vậy nồng độ phần trăm Ca(OH)2: 
Câu 2:
+ Khối lượng riêng  khối lượng dd H2SO4 là
khối lượng dd H2SO4 là 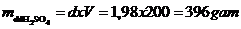
+ 
Số mol CuO: 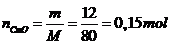
 Pt:
Pt: 

 Khối lượng
Khối lượng 
Vậy khối lượng chất tan: mct = 24 gam
Mà 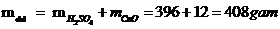
Vậy nồng độ phần trăm: 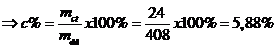

Theo đề bài ta có : ⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩VddH2O4=601,2=50(ml)nNaOH=20.20100.40=0,1(mol){VddH2O4=601,2=50(ml)nNaOH=20.20100.40=0,1(mol)
nFe = 1,68/56 = 0,03 mol
a) Ta có PTHH :
2NaOH + H2SO4 -> Na2SO4 + 2H2O
0,1mol......0,05mol
=> CMH2SO4 = 0,05/0,05=1(M)

\(n_{NaOH}=\frac{m}{M}=\frac{20}{40}=0,5mol\)
PTHH:
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,5 0,25 0,25 0,5 (mol)
b)\(m_{H_2SO_4}=n.M=0,25.98=24,5g\)
\(m_{ddH_2SO_4}=\frac{24,5.100}{20}=122,5g\)
c)\(m_{Na_2SO_4}=n.M=0,25.142=35,5g\)\(m_{ddNa_2SO_4}=m_{NaOH}+m_{ddH_2SO_4}=20+122,5=142,5g\)\(C\%_{Na_2SO_4}=\frac{35,5.100}{142,5}=24,91\%\)
PTHH: 2NaOH+H2SO4--->Na2SO4+2H2O
nNaOH = 20/40 = 0,5 (mol)
=>mH2SO4 = 0,25.98 = 24, 5 g
=> mddH2SO4 = 122,5g
=>mNa2SO4 = 0,25. 142 = 35,5g
=> mdd Na2SO4 = 142,5g
=>C%Na2SO4 = 24,91%

a) PTHH: CuO + H2SO4 ---> CuSO4 + H2O
b)
n Cu = 1,6 / 80 = 0,02 mol
m H2SO4 = 20 . 100 / 100 = 20 g
=> n H2SO4 = 20 / 98 = 0,204 mol
TPT:
1 mol : 1 mol
0,02 mol : 0,204 mol
=> Tỉ lệ: 0,02/1 < 0,204/1
=> H2SO4 dư, tính toán theo CuO
m dd sau p/ư = m dd H2SO4 + m CuO = 100 + 1,6 = 101,6 g
TPT: n CuSO4 = n CuO = 0,02 mol
=> m CuSO4 = 0,02 . 160 = 3,2 g
=> C% CuSO4 = 3,2 / 101,6 . 100% = 3,15%
n H2SO4 dư = 0,204 - 0,02 = 0,182 mol
=> m H2SO4 dư = 0,182 . 98 =17,836 g
=> C% H2SO4 = 17,836 / 101,6 . 100% = 17,83%

\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ FeO+H_2SO_4\rightarrow FeSO_4+H_2O\)
nH2=4,48/22,4=0,2(mol)
=>nFe=0,2(mol)=>mFe=0,2.56=11,2(g)
=>mFeO=18,4-11,2=7,2(g)
b)nH2SO4=nH2=0,2(mol)
=>mH2SO4 7%=0,2.98=19,6(g)
=>mH2SO4 =19,6:7%=280(g)
c)mFeSO4=0,2.152=30,4(g)
mdd sau pư=18,4+280-0,2.2=298(g)
=>C%FeSO4=\(\frac{30,4}{298}.100\%\)=10,2%

nH2SO4 =0,4 (mol)
nCuO = 0,2 (mol)
CuO + H2So4 -> CuSO4 + H2O
0,2........0,2 0,2 (mol)
H2SO4 dư 0,2 mol
\(C\%_{H2SO\text{4}}=\frac{0,2.98}{16+200}.100\%=9,\left(074\right)\%\)
C%CuSO4 = \(\frac{0,2.160}{16+200}.100\%=14,\left(814\right)\%\)

PTHH:SO3+H2O--->H2SO4
Ta có
n\(_{SO3}=\frac{16}{80}=0,2\left(mol\right)\)
Theo pthh
n\(_{H2SO4}=n_{SO3}=0,2\left(mol\right)\)
C\(_{M\left(H2SO4\right)}=\frac{0,2}{0,4}=0,5\left(M\right)\)
Chúc bạn học tốt
nSO3 = 0,2 mol
PTHH : SO3 +H2O--->H2SO4
=>nH2SO4 = 0,2 mol ( do nH2SO4 = nSO3)
=>CM = 0,2 / 0,4 = 0,5 M



a)nCuO=10:80=0,125(mol)
CuO+H2SO4->CuSO4+H2O
0,125...0,125.....0,125............(mol)
Theo PTHH:\(m_{H_2SO_4}\)=0,125.98=12,25(g)
=>\(C_{\%ddH_2SO_4}\)=\(\dfrac{12,25}{300}\).100%=4,1%
b)Theo PTHH:\(m_{CuSO_4}\)=0,125.160=20(g)
mà mdd(sau)=300+10=310(g)
=>\(C_{\%dd\left(sau\right)}\)=\(\dfrac{20}{310}\).100%=6,452%
a) PTHH: CuO + H2SO4 ----> CuSO4 + H2O
nCuO = \(\dfrac{10}{80}=0,125\left(mol\right)\)
Theo PTHH: n\(H_2SO_4\) = nCuO = 0,125 (mol)
=> m\(H_2SO_4\) = 0,125.98 = 12,25 (g)
=> C%\(H_2SO_4\) = \(\dfrac{12,25}{300}.100\%=4,08\%\)
b) Theo PTHH: n\(H_2O\) = nCuO = 0,125 (mol)
=> m\(H_2O\) = 0,125.18 = 2,25 (g)
=> mddsp/ứ = 10 + 300 - 2,25 = 307,75 (g)
Theo PTHH: n\(CuSO_4\) = nCuO = 0,125 (mol)
=> m\(CuSO_4\) = 0,125.160 = 20 (g)
=> C%\(CuSO_4\) = \(\dfrac{20}{307,75}.100\%=6,5\%\)