Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi x, y (mol) lần lượt là số mol Mg, Al trong hỗn hợp.
Phương trình phản ứng:
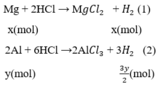
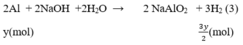
Số mol H2
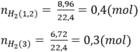
Theo bài ra ta có hệ phương trình:
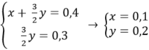
mMg = 24.0,1 = 2,4(g)
mAl = 27.0,2 = 5,4(g)

Đáp án A
Ta có: m(O) = 17,2 - 11,6 = 5,6
Suy ra n(O) = 0,35
Vậy n (HCl)= 0,7 nên m(muối)=11,6+0,7.35,5=36,45 gam

- Xét TN2:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,2<--------------------------------0,3
=> mAl = 0,2.27 = 5,4 (g)
- Xét TN1:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2------------------->0,3
Mg + 2HCl --> MgCl2 + H2
0,15<------------------0,15
=> mMg = 0,15.24 = 3,6 (g)

$2Al + 2H_2O + 2NaOH \to 2NaAlO_2 + 3H_2$
$n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{2}{3}. \dfrac{6,72}{22,4} = 0,2(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$n_{H_2} = \dfrac{3}{2}n_{Al} +n_{Mg}$
$\Rightarrow n_{Mg} = \dfrac{8,96}{22,4} - 0,2.\dfrac{3}{2} = 0,1(mol)$
Suy ra :
$m_{Mg} = 0,1.24 = 2,4(gam) ; m_{Al} = 0,2.27 = 5,4(gam)$

Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
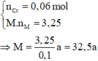
=> a = 2, M = 65 (M là Zn).

Chọn đáp án B
Gọi số mol mol mỗi kim loại là x mol
Khi cho X tác dụng HCl hình thành ZnCl2: x mol, CrCl2: x mol, SnCl2: x mol → 136x + 123x + 190x = 8,98 → x = 0,02 mol
Khi cho X phản ứng với O2 hình thành ZnO, Cr2O3, SnO2
Bảo toàn electron ta có nO2 pứ = ![]() = 0,045 mol → V = 1,008 lít.
= 0,045 mol → V = 1,008 lít.
⇒ Chọn B

Đáp án D
Đặt Zn, Cr,Sn là x mol → ZnCl2 : x mol, SnCl2 : x mol và CrCl2 : x mol
→ x =0,02 mol
Bảo toàn O trong phương trình đốt cháy có 2nO2 = x + 2x + 3/2 x =0,09
→ VO2= 1,008 lít

