Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cân bằng các phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
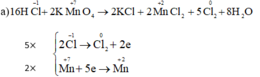
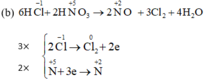
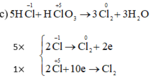
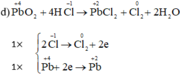
Tại sao chỉ tính oxi hóa của Cl2 mà ko tính oxi hóa của KCl vậy ạ?

(1) \(K\overset{+7}{Mn}O_4+H\overset{-1}{Cl}\rightarrow KCl+\overset{+2}{Mn}Cl_2+\overset{0}{Cl_2}+H_2O\)
- Chất khử: HCl
Chất oxh: KMnO4
- Sự oxh: \(2Cl^{-1}\rightarrow Cl_2^0+2e|\times5\)
Sự khử: \(Mn^{+7}+5e\rightarrow Mn^{+2}|\times2\)
\(\rightarrow2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
(2) \(H\overset{+5}{N}O_3+\overset{0}{Cu}\rightarrow\overset{+2}{Cu}\left(NO_3\right)_2+\overset{+4}{N}O_2+H_2O\)
- Chất khử: Cu
Chất oxh: HNO3
- Sự khử: \(N^{+5}+1e\rightarrow N^{+4}|\times2\)
Sự oxh: \(Cu^0\rightarrow Cu^{+2}+2e|\times1\)
\(\rightarrow4HNO_3+Cu\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\)
(3) \(\overset{-3}{N}H_3+\overset{0}{O_2}\rightarrow\overset{+2}{N}\overset{-2}{O}+H_2O\)
- Chất khử: NH3
Chất oxh: O2
- Sự khử: \(O_2^0+4e\rightarrow2O^{-2}|\times5\)
Sự oxh: \(N^{-3}\rightarrow N^{+2}+5e|\times4\)
\(\rightarrow4NH_3+5O_2\rightarrow4NO+6H_2O\)

1, 4Mg + 10HNO3 loãng------> 4Mg(NO3)2 + N2O + 5H2O
2, 10Al + 36HNO3 loãng------> 10Al(NO3)3 + 3N2 + 18H2O
3, 4Mg+ 10HNO3 loãng--------> 4Mg(NO3)2+ NH4NO3 + 3H2O
4, 3Fe3O4+ 28HNO3 loãng--------> .9Fe(NO3)3 +NO + 14H2O
5, 8FeS + 8 H2SO4 đặc------> 3Fe2(S04)3 + SO2+8H2
6, FeS2 + 18HNO3 đặc -------> Fe(NO3)3+ 15NO2 + 2H2SO4 + 7H2O
1, 4Mg+10HNO3 ----->4Mg(NO3)2+N2O+5H20
Quá trình khử: 2NO3− + 10H+ + 8e− = N2O + 5H
Quá trình oxy hoá Mg − 2e− = Mg2+

Bạn xem lại PT 1 và 3 nhé.
\(\overset{0}{Al}+H\overset{+5}{N}O_3\rightarrow\overset{+3}{Al}\left(NO_3\right)_3+\overset{0}{N_2}+H_2O\)
\(\overset{0}{Al\rightarrow}\overset{+3}{Al}+3e|\times10\)
\(2\overset{+5}{N}+10e\rightarrow\overset{0}{N_2}|\times3\)
⇒ 10Al + 36HNO3 → 10Al(NO3)3 + 3N2 + 18H2O
\(\overset{^{+2y/x}}{Fe_x}O_y+H\overset{+5}{N}O_3\rightarrow\overset{+3}{Fe}\left(NO_3\right)_3+\overset{+4}{N}O_2+H_2O\)
\(\overset{^{+2y/x}}{Fe_x}\rightarrow x\overset{+3}{Fe}+\left(3x-2y\right)e|\times1\)
\(\overset{+5}{N}+e\rightarrow\overset{+4}{N}|\times\left(3x-2y\right)\)
⇒ FexOy + (6x-2y)HNO3 → xFe(NO3)3 + (3x-2y)NO2 + (3x-y)H2O

1)\(K_2Cr_2O_7+HCl\rightarrow KCl+CrCl_3+Cl_2+H_2O\)
Có\(\left\{{}\begin{matrix}3\times|2Cl^{-1}\rightarrow Cl_2+2e\left(1\right)\\2\times|Cr^{+6}+3e\rightarrow Cr^{+3}\left(2\right)\end{matrix}\right.\)
\(\Rightarrow K_2Cr_2O_7+14HCl\rightarrow2CrCl_3+3Cl_2+2KCl+7H_2O\)Trong đó Cr là chất khử và Cl là chất oxi hóa, quá trình (1) là quá trình oxi hóa còn quá trình (2) là quá trình khử
2)\(P^0+H_2S^{+6}O_4\rightarrow H_3P^{+5}O_4+S^{+4}O_2+H_2O\)
Có:\(\left\{{}\begin{matrix}2\times|P^0\rightarrow P^{+5}+5e\left(1\right)\\5\times|S^{+6}+2e\rightarrow S^{+4}\left(2\right)\end{matrix}\right.\)
\(\Rightarrow2P+5H_2SO_4\rightarrow2H_3PO_4+5SO_2+2H_2O\)Trong đó S là chất khử, P là chất oxi hóa, quá trình (1) là quá trình oxi hóa còn quá trình (2) là quá trình khử
3)\(Mn^{+4}O_2+HCl^{-1}\rightarrow Mn^{+2}Cl_2+Cl^0_2+H_2O\)
Có\(\left\{{}\begin{matrix}1\times|Mn^{+4}+2e\rightarrow Mn^{+2}\left(1\right)\\1\times|2Cl^{-1}\rightarrow Cl_2^0+2e\left(2\right)\end{matrix}\right.\)
\(\Rightarrow MnO_2+4HCl\rightarrow MnCl_2+Cl_2+H_2O\)
Mn là chất khử còn Cl là chất oxi hóa, quá trình (1) là quá trình khử còn quá trình (2) là quá trình oxi hóa
4)\(Cu^0+HN^{+5}O_3\rightarrow Cu^{+2}\left(NO_3\right)_2+N^{+4}O_2+H_2O\)Có\(\left\{{}\begin{matrix}1\times|Cu^0\rightarrow Cu^{+2}+2e\left(1\right)\\2\times|N^{+5}+e\rightarrow N^{+4}\left(2\right)\end{matrix}\right.\)
\(Cu+4HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\)Cu là chất oxi hóa và N là chất khử, quá trình (1) là quá trình oxi hóa còn quá trình (2) là quá trình khử
a) Các quá trình
\(\overset{0}{Mg}\rightarrow\overset{+2}{Mg}+2e\)
\(\overset{+1}{2H}+2e\rightarrow\overset{0}{H_2}\)
\(\Rightarrow\) PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b) Các quá trình
\(2\overset{-3}{N}\rightarrow\overset{0}{N_2}+6e\) (Nhân với 1)
\(\overset{0}{Cl_2}+2e\rightarrow2\overset{-1}{Cl}\) (Nhân với 3)
\(\Rightarrow\) PTHH: \(2NH_3+3Cl_2\rightarrow N_2+6HCl\)
c) Các quá trình:
\(\overset{+5}{N}+1e\rightarrow\overset{+4}{N}\) (Nhân với 4)
\(\overset{0}{S}\rightarrow\overset{+4}{S}+4e\) (Nhân với 1)
\(\Rightarrow\) PTHH: \(4HNO_3+S\rightarrow SO_2+4NO_2+2H_2O\)