Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`- CaSO_4`
`K.L.P.T = 40 + 32 + 16.4 = 136 <am``u>`
\(\%Ca=\dfrac{40.100}{136}\approx29,41\%\)
`- CaCO_3`
`K.L.P.T = 40 + 12 + 16.3 = 100 <am``u>`
\(\%Ca=\dfrac{40.100}{100}=40\%\)
`- CaCl_2`
`K.L.P.T = 40 + 35,5.2=75,5 <am``u>`
\(\%Ca=\dfrac{40.100}{75,5}\approx52,98\%\)

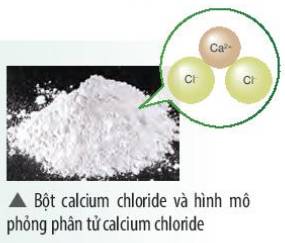
- Calcium chloride (CaCl2) có một số ứng dụng như: Làm hợp chất làm tan băng, làm chất điện giải hoặc sản xuất các loại đồ uống, có thể ứng dụng trong hệ thống tiêu nước và xử lí nước thải do công nghiệp thải ra.....
- Sơ đồ tạo thành liên kết trong Calcium chloride: 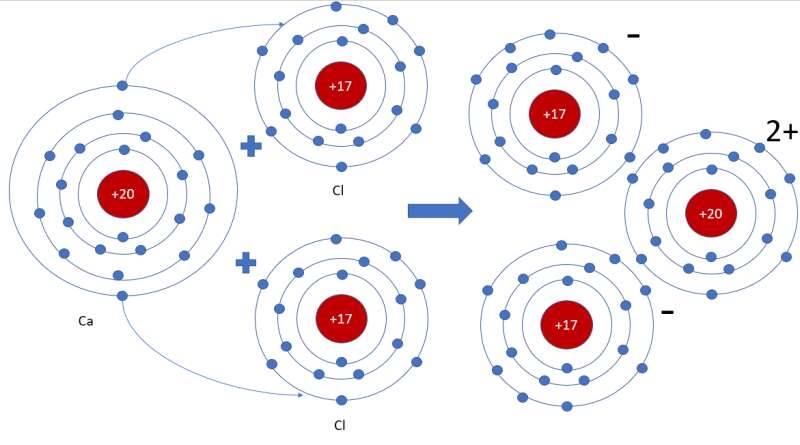

a, CTHH: CaSO4
b, MCaSO4 = 40 + 32 + 16.4 = 136 (g/mol)
\(\Rightarrow\left\{{}\begin{matrix}\%Ca=\dfrac{40}{136}.100\%\approx29,41\%\\\%S=\dfrac{32}{136}.100\%\approx23,53\%\\\%O\approx47,06\%\end{matrix}\right.\)

Gọi công thức hoá học của (T) là \(Ca_xC_yO_z\).
\(\%Ca=\dfrac{KLNT\left(Ca.x\right)}{KLPT\left(Ca_xC_yO_z\right)}.100\%=\dfrac{40x}{100}.100\%=40\%\Rightarrow x=1\)
\(\%C=\dfrac{KLNT\left(C.y\right)}{KLPT\left(Ca_xC_yO_z\right)}.100\%=\dfrac{12y}{100}.100\%=12\%\Rightarrow y=1\)
\(\%O=\dfrac{KLNT\left(O.z\right)}{KLPT\left(Ca_xC_yO_z\right)}.100\%=\dfrac{16z}{100}.100\%=48\%\Rightarrow z=3\)
Vậy công thức hoá học của (T) là: \(CaCO_3\)

- Thành phần chính của nước rửa tay khô là cồn ethanol: gồm 2 nguyên tử carbon, 6 nguyên tử hydrogen, 1 nguyên tử oxygen
=> Khối lượng phân tử của ethanol = 12 amu x 2 + 1 amu x 6 + 16 amu x 1 = 46 amu

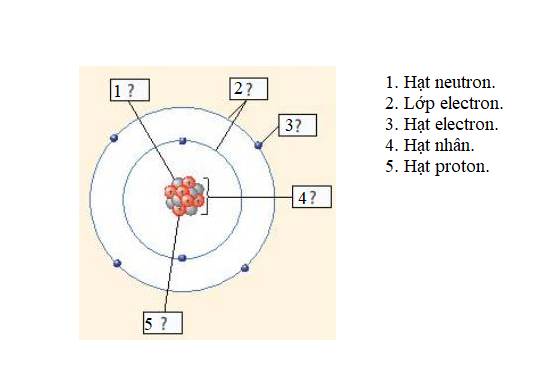
- 1 nguyên tử O góp chung 2 electron
=> 2 nguyên tử O góp chung 4 electron
- 1 nguyên tử S liên kết với 2 nguyên tử O
=> Si góp chung 4 electron
=> Nguyên tố Silicon có hóa trị IV
- Ứng dụng của silicon dioxide
+ Sản xuất kính cửa sổ, lọ thủy tinh
+ Lọc nước, xử lí nước tinh khiết
+ Sản xuất xi măng
+ Sản xuất đồ gốm
+ Góp phần sản xuất xà phòng và chất nhuộm màu

- Các mẫu chất potassium và iodine đều được tạo bởi phân tử đơn chất; potassium iodide tạo bởi phân tử hợp chất. Cụ thể:
+ Potassium (K) là đơn chất được tạo thành từ nguyên tố potassium (K).
+ Iodine (I2) là đơn chất được tạo thành từ nguyên tố iodine (I).
+ Potassium iodine (KI) là hợp chất được tạo thành từ nguyên tố potassium (K) và iodine (I)
Ứng dụng của iodine:
- Trong đời sống, iodine cung cấp dinh dưỡng cho con người, giúp giảm nguy cơ bệnh bướu cổ hay thiểu năng trí tuệ.
- Trong y học, iodine dùng làm thuốc sát khuẩn, thuốc trị bệnh bướu cổ, …
- Trong nông nghiệp, nó được dùng làm thuốc nuôi trồng thủy sản, phân bón, …
Ứng dụng của potassium iodine (KI):
- Trộn vào muối ăn để sản xuất muối I - ốt.
- Dùng bào chế thuốc điều trị cường giáp, nấm da, …
- Dùng trong cấy mô tế bào thực vật.
Potassium được tạo bởi phân tử K
Ứng dụng là phân bón, thuốc súng
Iodine được tạo bởi phân tử I2
Ứng dụng là thuốc sát trùng, phòng bệnh bướu cổ
Potassium được tạo bởi phân tử KI
Ứng dụng làm thuốc men, thực phẩm chức năng

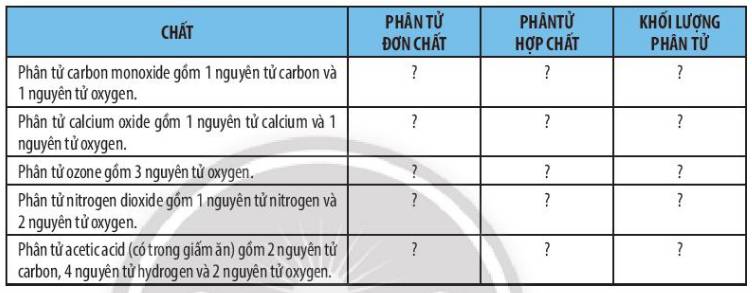
| Chất | Phân tử đơn chất | Phân tử hợp chất | Khối lượng phân tử |
| Phân tử carbon monoxide gồm 1 nguyên tử carbon và 1 nguyên tử oxygen | S | Đ | 28 |
| Phân tử calcium oxide gồm 1 nguyên tử calcium và 1 nguyên tử oxygen | S | Đ | 56 |
| Phân tử ozone gồm 3 nguyên tử oxygen | Đ | S | 48 |
| Phân tử nitrogen dioxide gồm 1 nguyên tử nitrogen và 2 nguyên tử oxygen | S | Đ | 46 |
| Phân tử acetic acid (có trong giấm ăn) gồm 2 nguyên tử carbon, 4 nguyên tử hydrogen và 2 nguyên tử oxygen | S | Đ | 60 |

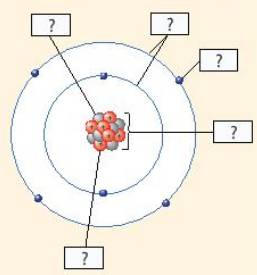
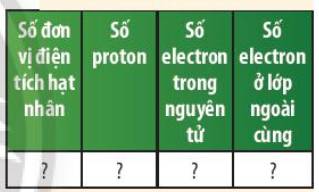
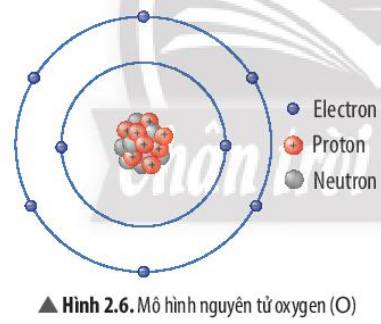



tham khảo
Bột thạch cao có nhiều ứng dụng quan trọng như: Tạo hình trong những công trình kiến trúc, làm vật liệu xây dựng, vữa trát tường, đúc tượng, làm khuôn đúc chịu nhiệt, … Trong y tế, nó còn được dùng làm khung xương, bó bột, khuôn mẫu trong nha khoa, …