Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(1,2H_2+O_2\underrightarrow{t}2H_2O\)
\(2Mg+O_2\underrightarrow{t}2MgO\)
\(2Cu+O_2\underrightarrow{t}2CuO\)
\(S+O_2\underrightarrow{t}SO_2\)
\(4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(C+O_2\underrightarrow{t}CO_2\)
\(4P+5O_2\underrightarrow{t}2P_2O_5\)
\(2,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(a,n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(b,n_C=0,3\left(mol\right)\Rightarrow n_{CO_2}=0,3\left(mol\right)\Rightarrow m_{CO_2}=13,2\left(g\right)\)
c, Vì\(\frac{0,3}{1}>\frac{0,2}{1}\)nên C phản ửng dư, O2 phản ứng hết, Bài toán tính theo O2
\(n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(3,PTHH:CH_4+2O_2\underrightarrow{t}CO_2+2H_2O\)
\(C_2H_2+\frac{5}{2}O_2\underrightarrow{t}2CO_2+H_2O\)
\(C_2H_6O+3O_2\underrightarrow{t}2CO_2+3H_2O\)
\(4,a,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_P=1,5\left(mol\right)\Rightarrow n_{O_2}=1,2\left(mol\right)\Rightarrow m_{O_2}=38,4\left(g\right)\)
\(b,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_C=2,5\left(mol\right)\Rightarrow n_{O_2}=2,5\left(mol\right)\Rightarrow m_{O_2}=80\left(g\right)\)
\(c,PTHH:4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(n_{Al}=2,5\left(mol\right)\Rightarrow n_{O_2}=1,875\left(mol\right)\Rightarrow m_{O_2}=60\left(g\right)\)
\(d,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(TH_1:\left(đktc\right)n_{H_2}=1,5\left(mol\right)\Rightarrow n_{O_2}=0,75\left(mol\right)\Rightarrow m_{O_2}=24\left(g\right)\)
\(TH_2:\left(đkt\right)n_{H_2}=1,4\left(mol\right)\Rightarrow n_{O_2}=0,7\left(mol\right)\Rightarrow m_{O_2}=22,4\left(g\right)\)
\(5,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=0,46875\left(mol\right)\)
\(n_{SO_2}=0,3\left(mol\right)\)
Vì\(0,46875>0,3\left(n_{O_2}>n_{SO_2}\right)\)nên S phản ứng hết, bài toán tính theo S.
\(a,\Rightarrow n_S=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_S=9,6\left(g\right)\)
\(n_{O_2}\left(dư\right)=0,16875\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=5,4\left(g\right)\)
\(6,a,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_C=1,5\left(mol\right)\Rightarrow m_C=18\left(g\right)\)
\(b,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_{H_2}=0,75\left(mol\right)\Rightarrow m_{H_2}=1,5\left(g\right)\)
\(c,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_S=1,5\left(mol\right)\Rightarrow m_S=48\left(g\right)\)
\(d,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_P=1,2\left(mol\right)\Rightarrow m_P=37,2\left(g\right)\)
\(7,n_{O_2}=5\left(mol\right)\Rightarrow V_{O_2}=112\left(l\right)\left(đktc\right)\);\(V_{O_2}=120\left(l\right)\left(đkt\right)\)
\(8,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(m_C=0,96\left(kg\right)\Rightarrow n_C=0,08\left(kmol\right)=80\left(mol\right)\Rightarrow n_{O_2}=80\left(mol\right)\Rightarrow V_{O_2}=1792\left(l\right)\)
\(9,n_p=0,2\left(mol\right);n_{O_2}=0,3\left(mol\right)\)
\(PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
Vì\(\frac{0,2}{4}< \frac{0,3}{5}\)nên P hết O2 dư, bài toán tính theo P.
\(a,n_{O_2}\left(dư\right)=0,05\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=1,6\left(g\right)\)
\(b,n_{P_2O_5}=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=14,2\left(g\right)\)

a)
Số mol photpho : 0,4 (mol).
Số mol oxi : 0,53 (mol).
Phương trình phản ứng :
4P + 5O2 -> 2P2O5
0,4 0,5 0,2 (mol)
Vậy số mol oxi còn thừa lại là :
0,53 – 0,5 = 0,03 (mol).
b) Chất được tạo thành là P2O5 . Theo phương trình phản ứng, ta có :
0,2 (mol).
Khối lượng điphotpho pentaoxit tạo thành là : m = 0,2.(31.2 + 16.5) = 28,4 gam.
a) PTHH: 4P + 5O2 -to-> 2P2O5
Ta có: \(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{17}{32}\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(\dfrac{0,4}{4}< \dfrac{\dfrac{17}{32}}{5}\)
=> P hết, O2 dư nên tính theo nP.
=> \(n_{O_2\left(phảnứng\right)}=\dfrac{5.0,4}{4}=0,5\left(mol\right)\\ =>n_{O_2\left(dư\right)}=\dfrac{17}{32}-0,5=\dfrac{1}{32}\left(mol\right)\)
b) Chất tạo thành sau phản ứng là P2O5 (điphotpho pentaoxit).
Theo PTHH và đề bài, ta có:
\(n_{P_2O_5}=\dfrac{2.0,4}{4}=0,2\left(mol\right)\)
Khối lượng P2O5 tạo thành sau phản ứng:
\(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)

Câu 1:
PTHH: Fe + 2HCl ===> FeCl2 + H2
a/ nFe = 11,2 / 56 = 0,2 mol
=> nH2 = 0,2 mol
=> VH2(đktc) = 0,2 x 22,4 = 4,48 lít
b/ => nHCl = 0,2 x 2 = 0,4 mol
=> mHCl = 0,4 x 36,5 = 14,6 gam
c/ => nFeCl2 = 0,2 mol
=> mFeCl2 = 0,2 x 127 = 25,4 gam
Câu 3/
a/ Chất tham gia: S, O2
Chất tạo thành: SO2
Đơn chất: S, O2 vì những chất này chỉ do 1 nguyên tố tạo nên
Hợp chất: SO2 vì chất này do 2 nguyên tố S và O tạo tên
b/ PTHH: S + O2 =(nhiệt)==> SO2
=> nO2 = 1,5 mol
=> VO2(đktc) = 1,5 x 22,4 = 33,6 lít
c/ Khí sunfuro nặng hơn không khí

1.
H2+ 1/2O2 --to> H2O
Mg + 1/2O2 --to> MgO
Cu+ 1/2O2--to>CuO
S+O2 --to>SO2
4Al+ 3O2--to>2Al2O3
C+ O2--to> CO2
2P+5/2O2--to> P2O5
b2
a)
C+O2to→CO2
nCO2=6,4\32=0,2
=>nCO2=nO2=0,2 mol
mCO2=0,2x44=8,8 g
b)
nC=6\12=0,5
nO2=19,2\32=0,6
C+O2to→CO2
TPU 0,5 0,6
PU 0,5 0,5 0,5
SPU 0 0,1 0,5
mCO2=0,5x44=22 g
b3
CH4+2O2to→CO2+2H2O
2C2H2+5O2to→4CO2+2H2O
C2H6O+3O2to→2CO2+3H2O
b4
a)
4P+5O2->2P2O5
nP=46,5/31=1,5 mol
=>nO2=1,5x5/4=1,875 mol
mO2=1,875x32=60 g
b)
nC=30/12=2,5 mol
C+O2->CO2
2,5 2,5
mO2=2,5x32=80 g
c)
nAl=67,5/27=2,5 mol
4Al+3O2->2Al2O3
2,5 1,875
mO2=1,875x32=60 g
d)
nH2=33,6/22,4=1,5 mol
2H2+O2->2H2O
1,5 0,75
mO2=32x0,75=24 g
b5
a,
nO2= 0,46875 mol
nSO2= 0,3 mol
S+ O2 -> SO2
=> O2 dư 0,16875 mol. Có 0,3 mol S cháy
mS= 9,6g
b,
mO2 dư= 5,4g
b6
CÓ nO2 = S/6.1023 = 3.1024 / 6. 1023 = 5 (mol)
=> VO2 = n x 22.4 = 5 x 22.4 =112(l)
b7
4P+5O2=to=>2P2O5
nP=6,2\31=0,2(mol);nO2=6,72\22,4=0,3(mol)
Theo PTHH, ta có: 0,2\4<0,3\5=>O2 dư
nO2(dư)=0,3−(0,2.5\4)=0,05(mol)
mO2(dư)=0,05.32=1,6(g)
nP2O5=2\4.nP=2\4.0,2=0,1(mol)
mP2O5=0,1.142=14,2(g)
b8
a. Số mol oxit sắt từ : nFe3O4=2,32\(56.3+16.4) = 0,01 (mol).
Phương trình hóa học.
3Fe + 2O2 -to> Fe3O4
3mol 2mol 1mol.
.................................... 0,01 mol.
Khối lượng sắt cần dùng là : m = 56.3.0,011=1,6856.3.0,01\1=1,68 (g).
Khối lượng oxi cần dùng là : m = 32.2.0,011=0,6432.2.0,01\1=0,64 (g).
b. Phương trình hóa học :
2KMnO4 to-> K2MnO4 + O2
2mol 1mol
n = 0,04 0,02
Số gam penmangarat cần dùng là : m= 0,04. (39 + 55 +64) = 6,32 g.
b9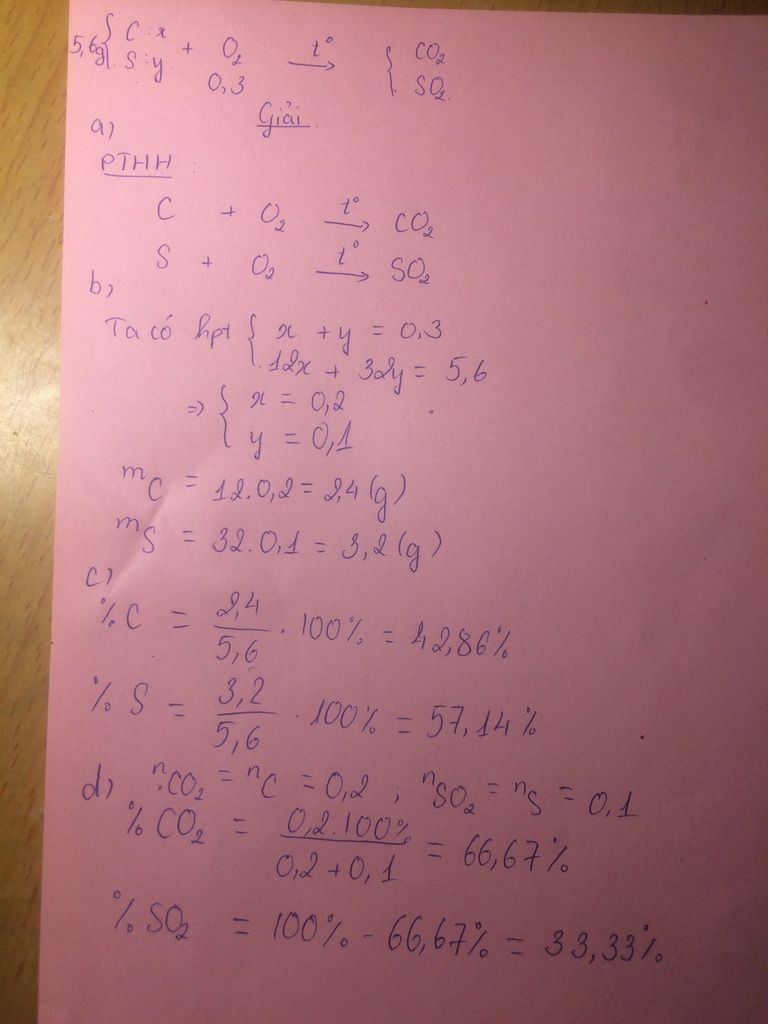
b11
a) PTHH: C + O2 → CO2 ↑
Đổi: 1 tấn = 1000000 gam
Khối lượng của C trong than là: 1000000.95% = 950000 gam
Số mol của C là: 950000:12 = 79166,67 mol
Số mol của O2 = 79166,67 mol
Khối lượng ôxi cần dùng là: 79166,67 . 32 = 2533333,44 gam

PTHH: 2C2H2 + 5O2 → 2H2O + 4CO2
VO2(đktc) = \(\frac{1,12\times20}{100}=0,244\left(lít\right)\)
=> nO2 = 0,224 / 22,4 = 0,01 (mol)
nC2H2 = 0,004(mol)
=> a = 0,004 x 26 = 0,104 (gam)
nH2O = 0,004 (mol)
=> mH2O = 0,004 x 18 = 0,072 (gam) = b
nCO2 = 0,008 (mol)
=> VCO2(đktc) = 0,008 x 22,4 = 0,1792(lít) = c

a)
nO2=8.96/22,4=0.4 mol
---->mO2=0.4*32=12.8g
nCO2=4.48/22.4=0.2 mol
---->mCO2=0.2*44=8.8g
Áp dụng định luật bảo toàn khối lượng:
mA+mO2=mCO2+mH2O
---->mA=mCO2+mH2O-mO2=8.8+7.2-12.8=3.2g
b) Gọi CTPT của A là CxHy
4CxHy + (4x+y)O2-----> 4xCO2 + 2yH2O
Ta có:
dMA/MHe=(12x+y)/4=4
---->MA=12x+y=16(1)
nCxHy=1/x*nCO2=0.2/x=3.2/16=0.2mol(2)
-----> x=1 ; y=4
Vậy CTPT của A là CH4

9
có phương trình: 4 P + 5 O2 → 2 P2O5 ( nhớ có nhiệt độ ấy nhé)
Áp dụng ĐLBTKL có: mP + m O2 = m P2O5
hay 3,1 + m O2 = 7,1 ↔ m O2 = 4 g
11
4P+5O2=to=>2P2O5
nP=6,2\31=0,2(mol);nO2=6,72\22,4=0,3(mol)
Theo PTHH, ta có: 0,2\4<0,3\5=>O2 dư
nO2(dư)=0,3−(0,2.54)=0,05(mol)
mO2(dư)=0,05.32=1,6(g)
nP2O5=2\4.nP=2\4.0,2=0,1(mol)
mP2O5=0,1.142=14,2(g)
12
Quan sát nhận xét: lưu huỳnh cháy trong k khí vs ngọn lửa nhỏ,màu xanh nhạt; cháy trong oxi mãnh liệt hơn,tạo thành khí lưu huỳnh đioxit SO2 và rất ít lưu huỳnh trioxit (S03)
PTHH: S+ 02--t°--SO2

theo định luật bảo toàn khối lương ta có :
mA + mO2 = mCO2 + mH2O
<=> 16 + 64 = mCO2 +H2O
<=> 80 = mCO2 +H2O
đặt 9x là mH2O => mCO2 =11x
ta có : 9x+ 11x= 80
giải tìm x= 4
=>mH2O= 36 g
=>mCO2= 44
Câu 1: Hợp chất B ở thể khí có công thức là: XO2. Biết khối lượng của 5,6l khí B (đktc) là 16g. Hãy xác định công thức của B.
A. CO2; B. SO2; C. NO2
bài giải
nRO2=V:22,4=5,6:22,4=0,25mol
MRO2=m:n=16:0,25=64g/mol
ta có R+2O=64
->R=32
VẬY R LÀ S(LƯU HUỲNH). CTHH : SO2
Câu 2: Đốt cháy 12 gam cacbon (C) trong bình kín chứa 11,2 lít khí oxi ở đktc. Chất còn dư sau phản ứng là cacbon (C), có khối lượng m gam. Giá trị m là:
A. 6,0 gam B. 5,0 gam C. 0,6 gam. D. 0,5 gam.
Đáp án:
A
Giải thích các bước giải:
nC = 12/12 = 1 mol ; nO2 = 11,2/22,4 = 0,5 mol
PTHH : C + O2 -> CO2
0,5 <- 0,5 mol
nC dư = 1 - 0,5 = 0,5 mol
-> mC = 0,5 *12 = 6 gam
Câu 3: Đốt 12,4 gam photpho (P) trong bình chứa khí oxi (O2) tạo thành mốt chất rắn, màu trắng là điphotpho pentaoxit (P2O5). Khối lượng hợp chất sau phản ứng thu được là:
A. 24,8 gam. B. 28,4 gam. C. 14,2 gam. D. 42,1 gam.
a) PTHH: 4P + 5O2 -to-> 2P2O5
Ta có: nP=12,4\31=0,4(mol)nO2=17\32(mol)
Theo PTHH và đề bài, ta có:
0,4\4<17\32\5
=> P hết, O2 dư nên tính theo nP.
=> nO2(phảnứng)=5.0,44=0,5(mol)=>nO2(dư)=1732−0,5=132(mol
b) Chất tạo thành sau phản ứng là P2O5 (điphotpho pentaoxit).
Theo PTHH và đề bài, ta có:
nP2O5=2.0,44=0,2(mol)nP2O5=2.0,44=0,2(mol)
Khối lượng P2O5 tạo thành sau phản ứng:
mP2O5=0,2.142=28,4(g)
Câu 4: Cho 9,6 gam khí oxi có thể dùng để đốt cháy vừa hết:
A. 0,1 mol C; B. 0,5 mol S; C. 0,2 mol H2; D. 0,4 mol Al
tham khảo mà quên xóa tên ng làm kìa cj