Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi A là công thức chung của 2 kim loại
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: A + 2HCl --> ACl2 + H2
____0,06<-------------------0,06
=> \(\overline{M}_A=\dfrac{2,24}{0,06}=37,333\)
Mà 2 kim loại thuộc nhóm IIA, 2 chu kì liên tiếp
=> 2 kim loại là Mg, Ca
b) nHCl = 0,5.0,4 = 0,2 (mol)
PTHH: Ca + 2HCl --> CaCl2 + H2
_____a------>2a-------->a------>a
Mg + 2HCl --> MgCl2 + H2
b----->2b-------->b
=> \(\left\{{}\begin{matrix}40a+24b=2,24\\a+b=0,06\end{matrix}\right.=>\left\{{}\begin{matrix}a=0,05\\b=0,01\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(CaCl_2\right)}=\dfrac{0,05}{0,5}=0,1M\\C_{M\left(MgCl_2\right)}=\dfrac{0,01}{0,5}=0,02M\\C_{M\left(HCl\right)}=\dfrac{0,2-2.0,05-2.0,01}{0,5}=0,16M\end{matrix}\right.\)

a)
Gọi công thức chung của 2 kim loại là X
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: X + 2HCl --> XCl2 + H2
0,4<------------------0,4
=> \(\overline{M}_X=\dfrac{12}{0,4}=30\left(g/mol\right)\)
Mà 2 kim loại thuộc nhóm IIA, liên tiếp nhau
=> 2 kim loại là Mg, Ca
b) Gọi \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Ca}=b\left(mol\right)\end{matrix}\right.\)
=> 24a + 40b = 12 (1)
Và a + b = 0,4 (2)
(1)(2) => a = 0,25 (mol); b = 0,15 (mol)
=> \(\left\{{}\begin{matrix}m_{Mg}=0,25.24=6\left(g\right)\\m_{Ca}=0,15.40=6\left(g\right)\end{matrix}\right.\)
c)
\(n_{HCl}=2.n_{H_2}=0,8\left(mol\right)\)
=> mHCl = 0,8.36,5 = 29,2 (g)
=> \(a=\dfrac{29,2.100}{18,25}=160\left(g\right)\)
d)
mdd sau pư = 12 + 160 - 0,4.2 = 171,2 (g)
\(n_{MgCl_2}=0,25\left(mol\right)\) => \(m_{MgCl_2}=0,25.95=23,75\left(g\right)\)
\(n_{CaCl_2}=0,15\left(mol\right)\) => \(m_{CaCl_2}=0,15.111=16,65\left(g\right)\)
=> \(\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{23,75}{171,2}.100\%=13,87\%\\C\%_{CaCl_2}=\dfrac{16,65}{171,2}.100\%=9,73\%\end{matrix}\right.\)

1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi \(\rightarrow\) (hỗn hợp oxit ) + axit \(\rightarrow\) muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=> \(n_O=\frac{9,6}{16}=0,6mol\)
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 \(\rightarrow\) xM + yH2O (1)
\(n_{H_2}=\frac{985,6}{22,4.1000}=0,044\left(mol\right)\)
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl \(\rightarrow\) 2MCln + nH2 (2)
\(n_{H_2}=\frac{739,2}{22,4.1000}=0,033\left(mol\right)\)
(2) => \(\frac{1,848}{M}.n=2.0,033\)
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1) \(\frac{x}{y}=\frac{n_M}{n_{H_2}}=\frac{0,033}{0,044}=\frac{3}{4}\)
=> oxit cần tìm là Fe3O4
1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi (hỗn hợp oxit ) + axit muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=>
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 xM + yH2O (1)
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl 2MCln + nH2 (2)
(2) =>
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1)
=> oxit cần tìm là Fe3O4

Đổi 896 cm3 = 0,896 lít
=> nH2 = 0,896 / 22,4 = 0,04 mol
Đặt công thức hóa học chung của 2 kim loại kiềm thổ là \(\overline{M}\)
PTHH: \(2\overline{M}+2H_2O\rightarrow2\overline{M}OH+H_2\)
0,08.........................................0,04
=> \(M_{\overline{M}}=\frac{2,16}{0,08}=27\left(\frac{g}{mol}\right)\)
=> Hai kim loại kiềm đó là Na và K
b/ Gọi số mol K, Na lần lượt là x, y (mol)
PTHH
2K + 2H2O ===> 2KOH + H2
x.............................................0,5x
2Na + 2H2O ===> 2NaOH + H2
y ................................................y
Theo đề ra, ta có hệ phương trình:
\(\begin{cases}39x+23y=2,16\\0,5x+0,5y=0,04\end{cases}\)
=> \(\begin{cases}x=0,02\\y=0,06\end{cases}\)
=> mNa = 0,06 x 23 = 1,38 gam
mK = 0,02 x 39 = 0,78 gam
=> %mNa = \(\frac{1,38}{2,16}.100\%=63,89\%\)
%mK = 100% - 63,89% = 36,11%
c/


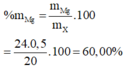
Câu 1:
Hợp chất KHí với Hidro: RH2
\(\Rightarrow\) Ngtố ∈ nhóm VIA \(\Rightarrow\) Oxit cao nhất: RO3
%O = 60% \(\Rightarrow\)%R = 40%
\(\Rightarrow\)\(\dfrac{\%R}{\%O}\)=\(\dfrac{1.M_R}{3.M_O}\)\(\Rightarrow\)\(\dfrac{\text{40%}}{60\%}\)=\(\dfrac{M_R}{3.16}\)\(\Rightarrow\)MR= 32 g/mol
\(\Rightarrow\)Ngtố S
b) Ta có C% =\(\dfrac{m_{ct}}{m_{dd}}\).100 \(\Rightarrow\)mct=\(\dfrac{C\%.m_{dd}}{100}\)= \(\dfrac{19,6.100}{100}\)=19,6 g
Mà mdd= mct + mdung môi \(\Rightarrow\)mdung môi=mdd - mct = 100 - 19,6 = 80,4g
Câu 2 THÌ MÌNH LƯỜI QUÁ :))