Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phát biểu sai: C
Khi phản ứng thuận nghịch đạt trạng thái cân bằng, nồng độ mol của chất phản ứng và các chất sản phẩm không đổi. Tùy thuộc vào hệ số tỉ lượng của phương trình phản ứng và thời điểm đạt trạng thái cân bằng, không phải lúc nồng độ mol của chất phản ứng cũng bằng nồng độ mol của chất sản phẩm phản ứng.

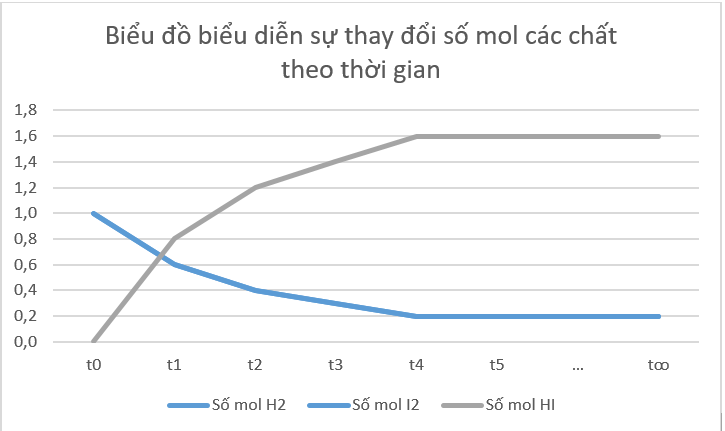
b) Từ đồ thị ta thấy: Lúc đầu số mol sản phẩm bằng 0, theo thời gian, số mol chất tham gia (hydrogen, iodine) giảm dần, số mol chất sản phẩm (hydrogen iodide) tăng dần, đến khi số mol của các chất hydrogen, iodine, hydrogen iodide không thay đổi nữa.
c) Biểu thức định luật tác dụng khối lượng:
- Đối với phản ứng thuận:
vthuận = \({\rm{k}}{\rm{.}}{{\rm{C}}_{{{\rm{H}}_{\rm{2}}}}}{\rm{.}}{{\rm{C}}_{{{\rm{I}}_{\rm{2}}}}}\)
- Đối với phản ứng nghịch:
vnghịch = \({\rm{k'}}{\rm{.C}}_{{\rm{HI}}}^2\)
Dự đoán:
- Ban đầu tốc độ phản ứng thuận giảm dần, sau một thời gian tốc độ phản ứng thuận không thay đổi theo thời gian.
- Ban đầu tốc độ phản ứng nghịch tăng dần, sau một thời gian tốc độ phản ứng nghịch không thay đổi theo thời gian.
d) Tại thời điểm phản ứng thuận nghịch đạt tới trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch thì số mol các chất trong hệ phản ứng không thay đổi nữa.

1. Phương trình hoá học của các phản ứng :
2 N H 3 + 3CuO → t ° N 2 + 3Cu + 3 H 2 O (1)
Chất rắn A thu được sau phản ứng gồm Cu và CuO còn dư. Chỉ có CuO phản ứng với dung dịch HCl :
CuO + 2HCl → C u C l 2 + H 2 O (2)
2. Số mol HCl phản ứng với CuO : n H C l = 0,02.1 = 0,02 (mol).
Theo (2), số mol CuO dư : n C u O = n H C l / 2 = 0,01 (mol).
Số mol CuO tham gia phản ứng (1) = số mol CuO ban đầu - số mol CuO dư = 0,03 (mol).
Theo (1) n N H 3 = 2 n C u O /3 = 0,02 (mol) và nN2 = n C u O /3 = 0,01 (mol).
Thể tích khí nitơ tạo thành : 0,01. 22,4 = 0,224 (lít) hay 224 ml.

1. Phản ứng thuận: CaCO3 + H2CO3 → Ca(HCO3)2
Phản ứng nghịch: Ca(HCO3)2 → CO2 + H2O + CaCO3

a, (1) 4P+5.O2->2.P2O5
(2) P2O5+4.NaOH->2.Na2HPO4+H2O
b, photpho có n=6,2:31=0,2 mol.dựa theo pt (1) thấy nP2O5=0,1mol.theo pt (2) thấy nNaOH=0,4mol vậy mNaOH=0,4.40=16 g vậy m(dd NaOH)=16:32%=50 g
c, theo pt (2) nNa2HPO4 =0,2 mol vậy mNa2HPO4=0,2.142=28,4 g
m(dd sau pư)=mP+m(dd NaOH)=6,2+50=56,2 g
=> C%(dd Na2HPO4)=28,4:56,2=50,53%

\(v_{thuận}=k_{thuận}\left[A\right]^a\left[B\right]^b\\ v_{nghịch}=k_{nghịch}\left[C\right]^c\left[D\right]^d\\\dfrac{k_{thuận}}{k_{nghịch}} =\dfrac{\left[C\right]^c\left[D\right]^dv_{thuận}}{\left[A\right]^a\left[B\right]^bv_{nghịch}}\)
aA+bB ⇌ cC + dD
- Tốc độ phản ứng thuận ở trạng thái cân bằng: \({{\rm{v}}_{\rm{t}}}{\rm{ = }}{{\rm{k}}_{\rm{t}}}{{\rm{(A)}}^{\rm{a}}}{{\rm{(B)}}^{\rm{b}}}\)
- Tốc độ phản ứng nghịch ở trạng thái cân bằng: \({{\rm{v}}_{\rm{n}}}{\rm{ = }}{{\rm{k}}_{\rm{n}}}{{\rm{(C)}}^{\rm{c}}}{{\rm{(D)}}^{\rm{d}}}\)
- Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch:
\(\begin{array}{l}{\rm{ }}{{\rm{v}}_{\rm{t}}}{\rm{ = }}{{\rm{v}}_{\rm{n}}}\\ \Leftrightarrow {{\rm{k}}_{\rm{t}}}{{\rm{(A)}}^{\rm{a}}}{{\rm{(B)}}^{\rm{b}}}{\rm{ = }}{{\rm{k}}_{\rm{n}}}{{\rm{(C)}}^{\rm{c}}}{{\rm{(D)}}^{\rm{d}}}\end{array}\)
\( \Rightarrow \)\(\frac{{{{\rm{k}}_{\rm{t}}}}}{{{{\rm{k}}_{\rm{n}}}}} = \frac{{{{{\rm{(C)}}}^{\rm{c}}}{{{\rm{(D)}}}^{\rm{d}}}}}{{{{{\rm{(A)}}}^{\rm{a}}}{{{\rm{(B)}}}^{\rm{b}}}}}\)
2. Phương trình hoá học của phản ứng xảy ra khi cho khí Cl2 tác dụng với nước:
Cl2(aq) + H2O(l) ⇌ HCl(aq) + HClO(aq)
Phản ứng thuận: Cl2 + H2O → HCl + HClO
Phản ứng nghịch: HCl + HClO → Cl2 + H2O
3. Đáp án C. vì phản ứng một chiều là phản ứng chỉ xảy ra một chiều, không có sự tạo lại chất ban đầu, nên phản ứng một chiều có thể xảy ra hoàn toàn hoặc không hoàn toàn. Ví dụ như phản ứng cháy là một phản ứng một chiều, có thể xảy ra hoàn toàn hoặc không hoàn toàn, tùy thuộc vào điều kiện phản ứng.