Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\\n_{Fe}=c\left(mol\right)\end{matrix}\right.\)⇒ 24a + 27b + 56c = 26,05(1)
\(Mg + 2HCl \to MgCl_2 + H_2\\ 2Al +6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = a + 1,5b + c = \dfrac{13,44}{22,4} = 0,6(2)\)
\(Mg + Cl_2 \xrightarrow{t^o} MgCl_2\\ 2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3\\ 2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Cl_2} = a + 1,5b + 1,5c = \dfrac{17,36}{22,4} = 0,775(3)\)
Từ (1)(2)(3) suy ra: a = 0,325 ; b = -0,05 ; c = 0,35
→ Sai đề.

Muối: ACln có A + 35,5n = 13,35/2,7/A = 4,94A hay A = 9n.
Vậy n = 3 và A = 27 (Al).
VCl2 = 1,5.0,1.22,4 = 3,36 lít.

mCl2= 13,35 - 2,7 = 10,65 g
nCl2= 10,65/71 = 0,15 mol
VCl2= 0,15 x 22.4 = ..... (lít)
2A + nCl2 -> 2ACln (n là hoá trị KLoai nhé)
nA= 0,15x2/n = 0,3/n (mol)
MA= 2,7 / (0,3/n) = 9n
Biện luận: n = 3 => MA= 27 => A là nhôm
Mấy cái này dễ lắm lắm đó bạn, học cho kĩ nhé chứ vầy mà k biết làm thì mình cũng k biết sao :)
bn đã nói vậy thì mình cũng nói thật . từ trước đến giờ mình có quen làm những bài tập tính toán về môn hóa như thế này đâu , minh ko hok giỏi hóa ![]()

\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
PTHH: 2Fe + 3Cl2 --to--> 2FeCl3
0,4-->0,6
MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
2,4<-------------0,6
=> \(n_{NaCl}=2,4\left(mol\right)\)
=> \(\%NaCl=\dfrac{2,4.58,5}{200}.100\%=70,2\%\)
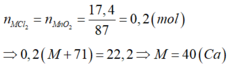
3)
Đơn chất halogen kí hiệu là X2
X2+ Ca\(\underrightarrow{^{to}}\) CaX2
nCaX2= \(\frac{10}{\text{40+ 2X}}\) mol
\(\rightarrow\) nX2= \(\frac{10}{\text{40+ 2X}}\) mol
2Al+ 3X2 \(\underrightarrow{^{to}}\) 2AlX3
Lượng halogen phản ứng là \(\frac{10}{\text{40+ 2X}}\) mol
\(\rightarrow\) nAlX3=\(\frac{20.\left(\text{40+ 2X}\right)}{3}\)= \(\frac{\text{800+40X}}{3}\) mol
Mà mAlX3= 8,9g \(\rightarrow\) nAlX3= \(\frac{8,9}{\text{27+ 3X}}\)
Ta có pt: \(\frac{\text{800+ 40X}}{3}\)= \(\frac{8,9}{\text{27+ 3X}}\)
\(\Leftrightarrow\) 26,7= \(\frac{\text{800+ 40X}}{3X+27}\)
\(\Leftrightarrow\) 26,7= 21600+ 2400X+ 1080X+ 120X2
\(\Leftrightarrow\) 120X2 + 3480X+ 21573,3= 0
PT ra 2 nghiệm âm nên ko có X thoả mãn đb
4)
C1: Khí clo màu vàng lục, oxi ko màu
C2: Đưa quỳ ẩm vào 2 khí. Clo làm quỳ hoá đỏ, sau đó mất màu. Oxi ko hiện tươngj
Cl2+ H2O\(⇌\) HCl+ HClO
C3: Dẫn 2 khí vào dd NaBr. Clo làm dd chuyển màu nâu đỏ. Oxi ko hiện tượng
Cl2+ 2NaBr\(\rightarrow\) 2NaCl+ Br2