Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

bài 3
Cu +2 AgNO3 -> Cu(NO3)2 + 2Ag
x...............2x.................................2x (mol)
theo bài ta có : 216x-64x=152x=2,28
==> x=0,015 (mol)=> n AgNO3=2x=0,03
==> CMAgNO3 =\(\dfrac{0,03}{\dfrac{30}{1000}}=1\left(M\right)\)
vậy............
bài 1
Zn + CuSO4 -> ZnSO4 + Cu
x x x (mol)
theo bài có 161x-160x=0,2==> x=0,2 = nZn
==> mZn tham gia = 0,2.65=13 (g)
vậy.........

* Nhận xét: “sau một thời gian phản ứng”, suy ra CuSO4 có thể vẫn còn dư. Gọi số mol Fe phản ứng là x mol.
a) Phương trình hóa học:
Fe + CuSO4 → FeSO4 + Cu
P/ư: x x x x mol
Khối lượng lá sắt tăng = 2,58 - 2,5 = 0,08 gam. Ta có phương trình:
64x - 56x = 0,08
x = 0,01 mol
b) Sô mol CuS04 ban đầu = 0,02625 mol
Trong dung dịch sau phản ứng có hai chất tan là FeSO4 0,01 mol và CuSO4 dư 0,01625 mol.
Khối lượng dung dịch:
mdd = + mFe(p.ư) – mCu = 25.1,12 + 0,01.56 - 0,01.64 = 27,91 g
C%, CuS04 = .100% ≈ 9,32%
C%, FeSO4 = .100% ≈ 5,45%
* Nhận xét: “sau một thời gian phản ứng”, suy ra CuSO4 có thể vẫn còn dư.
Gọi số mol Fe phản ứng là x mol.
a) Phương trình hóa học:
Fe + CuSO4 → FeSO4 + Cu
1 mol Fe phản ứng thì khối lượng sắt tăng: 64-56 = 8 gam
x mol Fe → 2,58 -2,5 = 0,08 gam
⇒ x = 0,01 mol
b) Số mol CuSO4 ban đầu
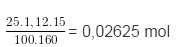
Trong dung dịch sau phản ứng có hai chất tan là FeSO4 0,01 mol và CuSO4 dư 0,01625 mol.
Khối lượng dung dịch:


PTHH: \(Mg+FeCl_2\rightarrow MgCl_2+Fe\)
Gọi \(n_{Mg\left(p.ứ\right)}=a\left(mol\right)=n_{Fe}\)
\(\Rightarrow36,8-24=56a-24a\) \(\Leftrightarrow a=0,4\) \(\Rightarrow\left\{{}\begin{matrix}m_{Mg\left(p.ứ\right)}=0,4\cdot24=9,6\left(g\right)\\m_{Fe}=0,4\cdot56=22,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{22,4}{36,8}\cdot100\%\approx60,87\%\\\%m_{Mg}=39,13\%\end{matrix}\right.\)

HD:
Fe + CuSO4 ---> FeSO4 + Cu
x x mol x x
a) Khối lượng Fe tăng lên = mCu (thoát ra) - mFe (tan vào dd) ---> 4%.50 = 64.x - 56x ---> x = 0,25 mol.
---> mCu = 64x = 64.0,25 = 16 gam.
b) [FeSO4] = 0,25/0,4 = 0,625 M; [CuSO4] = (0,4 - 0,25)/0,4 = 0,375 M.

Gọi x là số mol Zn p.ứ
Zn + CuSO4 = ZnSO4 + Cu
x x x (mol)
Vì khi phản ứng Zn tác dụng với CuSO4 và Cu bám trên bề mặt lá kẽm nên sau phản ứng ta thu được 49,82g khối lượng chất rắn gồm Zn dư và Cu
Ta có: 65x - 64x = 50 - 49,82 = 0,18(g)
=> x = 0,18 (mol)
Khối lượng CuSO4 trong dung dịch là
0,18 x 160 = 28,8 (g)
2. Cho 1,96g bột sắt vào 100ml dd CuSO4 10% có khối lượng riêng là 1,12g/ml
a)Viết ptpư
b) Xác định nồng độ mol/lit của các chất trong dd sau khi pư kết thúc
c) Cô cạn dd thu được bao nhiêu gam muối khan
---------
nFe= 1,96/56= 0,035(mol)
mddCuSO4= 100.1,12= 112(g)
=> mCuSO4= (112.10)/100= 11,2(g)
=> nCuSO4= 11,2/160= 0,07(mol)
PTHH: Fe + CuSO4 -> FeSO4 + Cu
Ta có: 0,035/1 < 0,07/1
=> Fe hết, CuSO4 dư, tính theo nFe
=> dd sau phản ứng gồm dd FeSO4 và dd CuSO4 dư.
Ta có: nCuSO4(p.ứ)= nFeSO4= nFe= 0,035(mol)
=> nCuSO4(dư)= 0,07 - 0,035= 0,035(mol)
Vddsau= VddCuSO4= 100(ml)= 0,1(l)
=> \(C_{MddCuSO_4\left(dư\right)}=\dfrac{0,035}{0,1}=0,35\left(M\right)\)
\(C_{MddFeSO_4}=\dfrac{0,035}{0,1}=0,35\left(M\right)\)
- Cô cạn dd dc 2 loại muối khan: CuSO4 (dư) và FeSO4.
m(muối_khan)= mCuSO4+ mFeSO4= 0,035.160 + 0,035.152= 10,92(g)
1/
Cu+ 2AgNO3 -----> Cu(NO3)2+ 2Ag
Khối lượng dd giảm: mdd↓=340*6%*25%=5.1
Ta luôn có mdd giảm=mKL tăng=5.1g
Khối lượng vật sau p/ư: mvật=15+5.1=20.1 g