Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCO2 =nCa(OH)2=6/100=0,06 mol=nCO pứ
nFe2O3=16/160=0,1 mol
=>nFe=0,2 mol
bảo toàn Fe nFe hh sau pứ=0,2 mol
bảo toàn klg=> m cr sau pứ=16+0,06.28-0,06.44=15,04 gam
GS hh cr sau pứ gồm Fe và O
=>mO=15,04-0,2.56=3,84 gam
=>nO=0,24 mol
khi cho hh cr tác dụng với H2SO4 đặc nóng
O +2e => O−2
0,24 mol=>0,48 mol
S+6 +2e => S+4
0,12 mol=>0,06 mol
Fe => Fe+3 +3e
0,2 mol =>0,6 mol
VSO2=0,06.22,4=1,344 lit
c giải cho e r mà?
nCO2=nCa(OH)2=6/100=0,06 mol=nCO
=>nFe=0,2 mol
bảo toàn ngtố Fe nFe hh sau pứ=0,2 mol
bảo toàn klg=> m cr sau pứ=16+0,06.28-0,06.44=15,04 gam
GS hh cr sau pứ gồm Fe và O
=>mO=15,04-0,2.56=3,84 gam
=>nO=0,24 mol
khi cho hh cr tác dụng với H2SO4 đặc nóng
O +2e => O-2
S+6 +2e => S+4
0,12 mol=>0,06 mol
Fe => Fe+3 +3e
0,2 mol =>0,6 mol
VSO2=0,06.22,4=1,344 lit
(lỗi kí tự hóa học)

nFe = 0,1 mol. m O2 = 7,36 - 5,6 = 1,76 gam => n O2 = 0,055 mol
Đặt nNO = x, nNO2 = y
Ta có hệ: bảo toàn electron: 3.0,1 - 0,055.4 = 3x + y
30x + 44y / ( x+y) = 19.2
=> x= 0,02, y =0,02
=> V = 0,04.22,4 = 8,96 lít

*Sơ đồ
\(Fe+O2->\left\{{}\begin{matrix}FeO\\Fe2O3\\Fe3O4\\Fe\end{matrix}\right.+HNO3->Fe^{3+}+NO+H2O\)
_Theo bài:
nFe =10,08/56 = 0,18 mol
_Theo BTKL có:
mO2 = mA - mFe = 12 - 10,08 = 1,92g
=>nO2 = 1,92/32 = 0,06
_Quá trình cho và nhận e:
Feo - 3e -> Fe+3
0,18...0,54
_______________________
N+5 + 3e ->N+2
.................3x.......x
O2o + 4e -> 2O-2
0,06.........0,24
_Theo bảo toàn e:
ne cho = ne nhận
=>0,54 = 3x + 0,24
=>x = 0,3/3 = 0,1
=>nNO = x = 0,1 mol
=> V = 0,1 . 22,4 = 2,24 lít

Theo đề bài ta có : nH2 = \(\dfrac{56}{22,4.1000}=0,0025\left(mol\right)\)
PTHH :
Fe + 2HCl - > FeCl2 + H2
0,0025mol......................0,0025mol
FeO + 2Hcl - > FeCl2 + H2O
Fe2O3 + 6HCl - > 2FeCl3 + 3H2O
=> %mFe = \(\dfrac{0,0025.56}{0,4}.100\%=35\%\)
=> %mFeO + %mFe2O3 = 65%
<=> mFeO + mFe2O3 = 0,65 (g)
Gọi nFeO = x , nFe2O3 = y
Ta có PTHH :
FeO + H2 -t0- > Fe + H2O
xmol.............................xmol
Fe2O3 + 3H2-t0-> 2Fe + 3H2O
ymol..................................3ymol
Ta có HPT : \(\left\{{}\begin{matrix}72x+160y=0,65\\x+3y=\dfrac{0,2115}{18}\end{matrix}\right.=>x=0,00125;y=0,0035\)
=> \(\left\{{}\begin{matrix}\%mFeO=\dfrac{0,00125.72}{1}.100\%=9\%\\\%mFe2O3=100\%-35\%-9\%=56\%\end{matrix}\right.\)
vậy...

\(n_{Fe_2O_3}=n_{FeO}=n_{Fe_3O_4}=a\\ n_{NO_2}:n_{NO}=\dfrac{46-34}{34-30}=3\\ n_{NO_2}+n_{NO}=\dfrac{4,48}{22,4}=0,2\\ n_{NO_2}=0,15;n_{NO}=0,05\\ BTe:a+a=0,15+0,15\\ a=0,15\\ m_A=a\left(160+232+72\right)=69,6g\\ BT\left[N\right]:V_{HNO_3}=\dfrac{6a\cdot3-0,2}{2}=1,25L\)


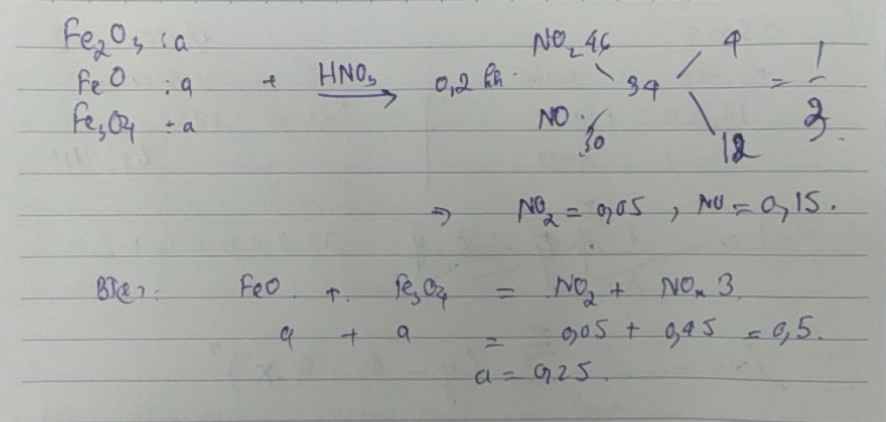
-Cho vào dd H2SO4(l) dư
+)Nếu có khí thoát ra:Fe
Fe+H2SO4⇒FeDO4+H2
+)Các khí còn lại 0 hiện tượng
-Cho các khí còn lại vào dd NaOH dư:
+)Mẫu xuất hiện kết tủa nâu đỏ:Fe2O3
+)Mẫu xuất hiện kết tủa trắng xanh và hóa nâu đỏ trong không khí:Fe
+)Mẫu vừa xuất hiện kết tủa trắng xanh vừa xuất hiện kết tủa nâu đỏ và hóa nâu đỏ trong không khí:Fe3O4