Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải:
1) Khối lượng của NaCl có trong 1 kg NaCl bão hòa là:
\(\dfrac{S}{S+100}\) = \(\dfrac{mct}{mddbãohoa}\)
⇔ \(\dfrac{35,9}{35,9+100}\) = \(\dfrac{mct}{1000}\)
⇔ 135,9 . mct = 35,9 . 1000
⇔ 135,9mct = 35900
⇔ mct = 35900 : 135,9
⇔ mct ≈ 264,16 g
Vậy...
2) Độ tan của Na2SO4 ở 10oC là:
SNa2SO4 = \(\dfrac{mct.100}{m_{nước}}\) = \(\dfrac{7,2.100}{80}\) = 9 g
Nồng độ % của dd Na2SO4 ở 10oC là:
C% = \(\dfrac{S.100\%}{100+S}\) = \(\dfrac{9.100\%}{100+9}\) ≈ 8,26%
Vậy...

a, Ta có: $m_{CaSO_4}=0,2(g);m_{H_2O}=100(g)$
$\Rightarrow \%C_{CaSO_4}=0,2\%$
Mặt khác $V_{ddCaSO_4}=100,2(ml)\Rightarrow C_{M/CaSO_4}=0,015M$
b, Ta có: $n_{CaCl_2}=0,006(mol);n_{Na_2SO_4}=0,002(mol)$
$\Rightarrow n_{CaSO_4}=0,002(mol)\Rightarrow m=0,272(g)$
Giả sử 200ml dung dịch là $H_2O$ $\Rightarrow m_{dd}=200(g)$
So sánh với độ tan của $CaSO_4$ thì không có kết tủa xuất hiện

a)
Ở 50oC,
37 gam NaCl tan tối đa trong 100 gam nước tạo thành 137 gam dung dịch
x...gam NaCl tan tối đa trong 100 gam nước tạo thành 411 gam dung dịch
\(\Rightarrow x = \dfrac{411.37}{137} = 111(gam)\)
b)
- Ở 50oC ,
37 gam NaCl tan tối đa trong 100 gam nước tạo thành 137 gam dung dịch
a...gam NaCl tan tối đa trong b.....gam nước tạo thành 548 gam dung dịch
\(\Rightarrow a = \dfrac{548.37}{137} = 148(gam)\\ \Rightarrow b = \dfrac{548.100}{137} = 400(gam)\)
- Ở 0oC,
35 gam NaCl tan tối đa trong 100 gam nước tạo thành 135 gam dung dịch
c...gam NaCl tan tối đa trong 400 gam nước tạo thành dung dịch bão hòa
\(\Rightarrow c = \dfrac{400.35}{100}= 140(gam)\)
Vậy :
\(m_{NaCl\ kết\ tinh} = a - c = 148 - 140 = 8(gam)\)

Theo đề : SNa2CO3(20o)= 21,5 gam, ta có:
m Na2CO3 = 243 x (21,5/121,5) = 43 gam; mH2O= 243 - 43 = 200 gam
Ở 90oC, SNa2CO3= 43,9 gam, ta có:
Cứ 100 gam nc hòa tan đc 43,9 gam Na2CO3
Vậy 200 gam ns___________ > 87,8 gam Na2CO3
Để dd bão hòa ở 90o thì phải thêm 1 lượng K2CO3 là:
mK2CO3( cần thêm)= 87,8 - 43 = 44,8 gam

\(a.C_M=\dfrac{0,06}{1,5}=0,04M\\ b.C_M=\dfrac{\dfrac{400}{160}}{4}=0,625M\\ c.C_M=\dfrac{\dfrac{10,53}{58,5}}{\dfrac{450}{1,25}:1000}=0,5M\\ d.C_M=\dfrac{\dfrac{70,2}{40}}{0,5}=3,51M\\ e.C_M=\dfrac{\dfrac{42}{200}}{\dfrac{742}{1,3}:1000}=0,368M\)

/ nồng độ dung dịch KAl(SO4)2 bão hòa ở 20 độ C là 5,66%=> 600g dd KAl(SO4)2 chứa 600*5,66%=33,96g KAl(SO4)2 và 600-33,96g=566,04g H2O
độ tan = (33,96*100)/566,04=5,9996
b/ mH2O còn lại = 566,04-200=366,04g
nKAl(SO4)2=33,96/258 (mol)
nH2O=336,04/18(mol)
KAl(SO4)2 + 12H2O --->KAl(SO4)2.12H2O
33,96/258--------336,04/18
=> H2O dư
=>nKAl(SO4)2.12H2O=nKAl(SO4)2=33,96/25...
=>mKAl(SO4)2.12H2O=33,96/258*474=62,39...
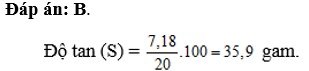
Câu 2:
7,2g Na2O4 thì hoà tan trong 80 gam H2O---> dung dịch bão hoà
=> xg Na2O4 thì hào tan trong 100g H2O--->dung dịch bão hoà
x = (100X7,2):80 = 9g
Vậy độ tan của Na2O4 ở 10 độ C trong nước là 9g.
C%=9/(9+100)=8,26%
Giải:
1) Khối lượng của NaCl có trong 1 kg NaCl bão hòa là:
\(\dfrac{S}{S+100}\) = \(\dfrac{m_{ct}}{m_{ddbãohòa}}\)
⇔ \(\dfrac{35,9}{35,9+100}\) = \(\dfrac{mct}{1000}\)
⇔ 135,9 . mct = 35,9 . 1000
⇔ 135,9mct = 35900
⇔ mct = 35900 : 135,9
⇔ mct ≈ 264,16 g
Vậy...
2) Độ tan của Na2SO4 ở 10oC là:
SNa2SO4 = \(\dfrac{mct.100}{m_{nước}}\) = \(\dfrac{7,2.100}{80}\) = 9 g
Nồng độ % của dd Na2SO4 ở 10oC là:
C% = \(\dfrac{S.100\%}{100+S}\) = \(\dfrac{9.100\%}{100+9}\) ≈ 8,26%
Vậy...