Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Giải
a) Gọi CTHH của oxit sắt là: FexOy
PTHH: : FexOy + yCO ------> xFe + yCO2
Số mol Fe là

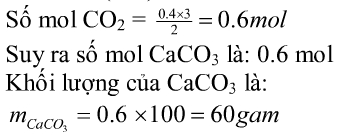
a/
mFe=22,4g
=> mO = 32-22,4=9,6g
Gọi công thức oxit sắt: FexOy
x:y=(22,4:56):(9,6:16)=2:3
=> CT: Fe2O3.
b/
nO=nC=nCO2=(9,6:16)=0,6mol
nCaCO3 =nCO2=0,6mol
=> mCaCO3 =0,6.100=60g

a) Gọi CTHH của oxit sắt là $Fe_2O_n$
$Fe_2O_n + nCO \xrightarrow{t^o} 2Fe +nCO_2$
$n_{Fe} = \dfrac{22,4}{56} = 0,2(mol)$
$\Rightarrow n_{Fe_2O_n} = \dfrac{1}{2}n_{Fe} = 0,2(mol)$
$M_{oxit} = 56.2 + 16n = \dfrac{32}{0,2}=160$
Suy ra : n = 3
Vậy oxit cần tìm là $Fe_2O_3$
b) $n_{CO_2} = \dfrac{3}{2}n_{Fe} = 0,6(mol)$
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,6(mol)$
$m_{CaCO_3} = 0,6.100 = 60(gam)$

1/dãy các phi kim tác dụng với nhau:
A.Si,Cl2,O2; B.H2,S,O2; C.Cl2,C,O2; D.N2,S,O2
2/dãy các phi kim được sắp xếp theo chiều hoạt động hóa học tăng dần
A.Br,Cl,F,I; B.I,Br,Cl,F; C.F,Br,I,Cl; D.F,Cl,Br,I
3/cho sơ đồ sau:MnO2-->X-->FeCl3-->Fe(OH)3. X là gì
A.Cl2; B.HCl; C.H2SO4; D.H2
4/đốt cháy 11,2l CO (đktc) . thể tích khí cần cho phản ứng trên là
A.21,4l B.24l C.26l D.28l
5/cho 1 mol Ca(OH)2 phản ứng với 1 mol CO2 . muối tạo thành :
A.CaCO3; B.Ca(HCO3)2; C.CaCO3 và Ca(HCO3)2; D.CaCO3 và Ca(OH)2 dư
6/để tạo muối KHCO3 duy nhất thì tỉ lệ CO2 sục vào dung dịch KOH là bao nhiêu ?
A.2:3 B.1:2 C.1:1 D.1:3
II/tự luận
1/cho 8,7g MnO2 tác dụng với axit HCl dư .Sau phản ứng thu được 1,9l khí clo (đktc).tính hiệu suất của phản ứng ?
2/tính khối lượng của Fe thu được khi cho một lượng CO dư khử 32g Fe2o3 . biết rằng hiệu suất phản ứng là 80%
3/a)hãy xác định công thức của một loại oxit sắt biết rằng khi cho 32g oxit sắt này tác dụng hoàn toàn với cacbon oxit thì thu được 22,4 chất rắn . biết khối lượng mol phân tử của oxit sắt là 160g/mol
b)chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong . tính khối lượng kết tủa thu được
1)
nMnO2= 8,7/87 = 0,1 mol
MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
0,1 0,1 (mol)
V Cl2 = 0,1 x 22,4 = 2,24 lít
H%=1,9/2,24x100%= 85%
pt:
Fe2O3+3CO---t*--->2Fe+3CO2
mFe2O3 p/ứ=32.80%=25,6(g)
=>nFe2O3=25,6/160=0,16(mol)
Theo pt: nFe=2nFe2O3=2.0,16=0,32(mol)
=>mFe=0,32.56=17,92(g)
bài 3
mFe=22,4g
=> mO = 32-22,4=9,6g
Gọi công thức oxit sắt: FexOy
x:y=(22,4:56):(9,6:16)=2:3
=> CT: Fe2O3.
b/
nO=nC=nCO2=(9,6:16)=0,6mol
nCaCO3 =nCO2=0,6mol
=> mCaCO3 =0,6.100=60g



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)




Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 0,25.........0,5.........0,25.......0,25\left(mol\right)\\ a.V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b.m_{HCl}=0,5.36,5=18,25\left(g\right)\\ c.n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\\ Fe_2O_3+3H_2\underrightarrow{^{to}}2Fe+3H_2O\\ Vì:\dfrac{0,25}{3}< \dfrac{0,1}{1}\\ \Rightarrow Fe_2O_3dư\\ n_{Fe}=\dfrac{2}{3}.0,25=\dfrac{1}{6}\left(mol\right)\\ \Rightarrow m_{Fe}=\dfrac{1}{6}.56\approx9,333\left(g\right)\)
a,\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,25 0,5 0,25
\(\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
b,\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
c,\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,25 \(\dfrac{1}{6}\)
Ta có: \(\dfrac{0,1}{1}>\dfrac{0,25}{3}\)⇒ Fe2O3 dư, H2 hết
\(m_{Fe}=\dfrac{1}{6}.56=9,33\left(g\right)\)

a)
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe +3 CO_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$RO + H_2 \xrightarrow{t^o} R + H_2O$
b)
Coi m = 160(gam)$
Suy ra: $n_{Fe_2O_3} = 1(mol)$
Theo PTHH :
$n_{RO} = n_{H_2} = n_{Fe} = 2n_{Fe_2O_3} = 2(mol)$
$M_{RO} = R + 16 = \dfrac{160}{2} = 80 \Rightarrow R = 64(Cu)$
Vậy oxit là CuO

1
nMnO2= 8,7/87 = 0,1 mol
MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
0,1 ------------------------------- 0,1 (mol)
V Cl2 = 0,1 x 22,4 = 2,24 lít
H%=1,9/2,24x100%= 85%
2
pt:
Fe2O3+3CO---t*--->2Fe+3CO2
mFe2O3 p/ứ=32.80%=25,6(g)
=>nFe2O3=25,6/160=0,16(mol)
Theo pt: nFe=2nFe2O3=2.0,16=0,32(mol)
=>mFe=0,32.56=17,92(g)
3
a) Gọi CTHH của oxit sắt là: FexOy
PTHH: : FexOy + yCO ------> xFe + yCO2
Số mol Fe là
@ tran gia vien