Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Công thức hóa học: S x O y
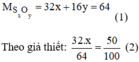
Giải phương trình (2) ta được: x = 1 thay vào pt (1) ⇒ y = 2.
Vậy công thức hóa học của oxit là S O 2

\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=\dfrac{64.50}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2

1.\(\dfrac{m_{Al}}{m_O}=\dfrac{9}{8}\)
\(Al_xO_y\)
\(x:y=\dfrac{9}{27}:\dfrac{8}{16}=\dfrac{1}{3}:\dfrac{1}{2}=2:3\)
Vậy CTHH là \(Al_2O_3\)
2.\(\rightarrow\%S=100-60=40\%\)
\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
Vậy CTHH là \(SO_3\)
3.
a.b.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=2.0,2=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,4 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
Chất dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,2\right).98=19,6g\)
c.Nồng độ gì bạn nhỉ?

Câu 1 :
\(M_{K_2CO_3}=39.2+12+16.3=138\left(dvC\right)\)
\(\%K=\dfrac{39.2}{138}.100\%=56,52\%\)
\(\%C=\dfrac{12}{138}.100\%=8,69\%\)
\(\%O=100\%-56,52\%-8,69\%=34,79\%\)
Còn lại cậu làm tương tự nhá

Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)

Gọi CTHH là SxOy
=> mS = \(\frac{64.50}{100}=32\left(gam\right)\)
\(\Rightarrow n_S=\frac{32}{32}=1\left(mol\right)\)
=> mO = 64 - 32 = 32 (gam)
=> nO = \(\frac{32}{16}=2\left(mol\right)\)
=> x : y = 1 : 2
=> CTHH: SO2
Gọi công thức dạng tổng quát cuả oxit đólà SxOy (x,y: nguyên, dương)
=>\(m_S=\frac{64.50}{100}=32\left(g\right)\)
\(n_S=\frac{m_S}{M_S}=\frac{32}{32}=1\left(mol\right)\)
=>\(m_O=m_{hợpchất}-m_S=64-32=32\left(g\right)\)
\(n_O=\frac{m_O}{M_O}=\frac{32}{16}=2\left(mol\right)\)
=>x:y=1:2
CTHH của oxit: SO2 (lưu huỳnh đioxit)

Bài 1:
+9,6 g khí oxi.
\(n_{O2}=\frac{9,6}{32}=0,3\left(mol\right)\)
\(2KMnO4-->K2MnO4+MnO2+O2\)
0,6<------------------------------------------------0,3(mol)
\(m_{KMnO4}=0,6.158=94,8\left(g\right)\)
\(2KClO3-->2KCl+3O2\)
0,2-----------------------------------0,3(mol)
\(m_{KClO3}=0,2.122,5=24,5\left(g\right)\)
+26,88 lít khí oxi ở đktc.
\(n_{O2}=\frac{26,88}{22,4}=1,2\left(mol\right)\)
\(2KMnO4-->K2MnO4+MnO2+O2\)
2,4------------------------------------------------1,2(mol)
\(m_{KMnO4}=2,4.158=379,2\left(g\right)\)
\(2KClO3-->2KCl+3O2\)
0,8<----------------------------1,2(mol)
\(m_{KClO3}=0,8.122,5=98\left(g\right)\)
Bài 2: Nung nóng 20 g KMnO4 một thời gian thấy khối lượng hỗn hợp chất rắn còn lại là 17,12 gam. Hãy tính khối lượng mỗi chất trong hỗn hợp chất rắn sau phản ứng.
\(m_{O2}=m_{KMnO4}-m_{cr}=20-17,12=2,88\left(g\right)\)
\(n_{O2}=\frac{2,88}{32}=0,09\left(mol\right)\)
\(2KMnO4-->K2MnO4+MnO2+O2\)
\(n_{K2MnO4}=n_{O2}=0,09\left(mol\right)\)
\(m_{K2MnO4}=0,09.197=17,73\left(g\right)\)
đề hơi sai sai??

Coi: mS = 2a (g) ⇒ mO = 3a (g)
\(\Rightarrow n_S=\dfrac{2a}{32}=\dfrac{a}{16}\left(mol\right)\)
\(n_O=\dfrac{3a}{16}\left(mol\right)\)
Gọi CTHH cần tìm là SxOy.
\(\Rightarrow x:y=\dfrac{a}{16}:\dfrac{3a}{16}=1:3\)
Vậy: CTHH cần tìm là SO3.
Gọi x, y lần lượt là số ml của S và O
Do tỉ lệ số mol của các chất chình là tỉ lệ giữa sô phân tử của nguyên tố cấu tạo nên chất
⇒ Công thức tổng quát SxOy
Theo đề bài, ta có: mS/mO = 2/3
=> 32x/16y = 2/3
=> 96/x = 32/y
=> x/y = 32/96 = 1/3
=> x = 1;
y = 3
=> Công thức hóa học: SO3

a)CTDC: SOx
\(\%S=40\%\)
\(\Rightarrow\frac{32}{32+16x}.100\%=40\%\)
\(\Leftrightarrow\frac{32}{32+16x}=0,4\)
\(\Leftrightarrow32=12,8+6,4x\)
\(\Rightarrow x=3\)
PTKl 60 đvc
=>CTHH:SO3
b) \(S+O2-->SO2\)
1) \(n_{SO2}=\frac{4}{64}=0,0625\left(mol\right)\)
\(n_S=n_{O2}=n_{SO2}=0,0625\left(mol\right)\)
\(m_S=0,0625.32=2\left(g\right)\)
\(V_{O2}=0,0625.22,4=1,4\left(l\right)\)
2) \(n_{SO2}=\frac{72}{64}=1,125\left(mol\right)\)
\(n_S=n_{O2}=n_{SO2}=1,125\left(mol\right)\)
\(m_S=1,125.32=36\left(g\right)\)
\(V_{O2}=1,125.22,4=25,2\left(l\right)\)
3) \(1kg=1000g\)
\(n_S=n_{O2}=n_{SO2}=\frac{1000}{64}=15,625\left(mol\right)\)
\(m_S=15,625.32=500\left(g\right)\)
\(V_{O2}=15,625.22,4=350\left(l\right)\)
4) \(n_S=n_{O2}=n_{SO2}=\frac{11,2}{22,4}=0,5\left(mol\right)\)
\(m_S=0,5.32=16\left(g\right)\)
\(V_{O2}=0,5.22,4=11,2\left(l\right)\)
a) Câu a sai đề
b) Vì sai đề nên sẽ không làm được câu b
Em chú ý lại các số giúp anh nhé!