Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

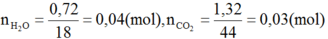
⇒ nH2O > nCO2
⇒ A là ancol no và theo đầu bài là đơn chức
Gọi công thức phân tử của A là CnH2n+2O (n ≥ 1)
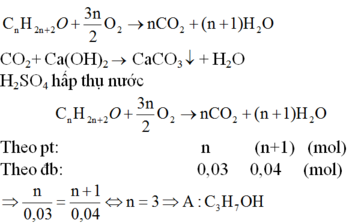

Khi cho A tác dụng với CuO, đun nóng được một anđehit ⇒ A là Ancol bậc 1
⇒ CTCT của A là: CH3-CH2-CH2-OH (propan-1-ol)

\(m_{H_2O}=10.8\left(g\right)\)
\(n_{H_2O}=\dfrac{10.8}{18}=0.6\left(mol\right)\)
\(m_{CO_2}=19.8\left(g\right)\)
\(n_{CO_2}=\dfrac{19.8}{44}=0.45\left(mol\right)\)
\(n_C:n_H=0.45:1.2=3:8\)
\(CT:C_3H_8O\)
\(C_3H_8O+CuO\rightarrow C_3H_6O+Cu+H_2O\)
\(X:\text{Propanal }\)

Đáp án : B
Theo đề bài, suy ra nH2O = 0,04 mol ; nCO2 = 0,03 mol
=> A là ancol no, nA = nH2O - nCO2 = 0,01 mol
=> MA = 60 (C3H7OH)

Khối lượng bình (1) tăng 0,63g chính là khối lượng H2O.
\(\Rightarrow m_H=\frac{0,63}{18}.2=0,07g\)
Ở bình (2) : \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
\(0,05\leftarrow\frac{5}{100}=0,05\)
\(\Rightarrow m_C=0,05.12=0,6g\)
\(\Rightarrow m_O=0,67-\left(m_C+m_H\right)=0\)
\(\Rightarrow\%m_C=\frac{0,6}{0,67}.100=89,55\%\)
\(\%m_H=100\%-89,55\%=10,45\%\)
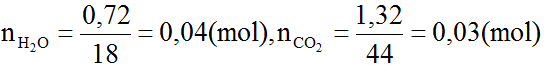

CTCT có thể có của A là:
CH3-CH2-CH2-OH, CH3-CH(OH)-CH3