Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H^+} = n_{HCl} + n_{HNO_3} = 0,4 + 0,4.1,2 = 0,88\)
\(Gọi\ n_{Fe} = a ;n_O = b ; n_{NO} = c\)
Suy ra :
56a + 16b = 12,48(1)
Bảo toàn electron : 3a = 2b + 3c(2)
\(n_{H^+\ pư} = 2n_O + 4n_{NO} = 2b + 4c(mol)\\ n_{H^+\ dư} = 0,88 - 2b - 4c\)
\(2Fe^{3+} + Cu \to Cu^{2+} + 2Fe^{2+}\\ 3Cu + 8H^+ + 2NO_3^- \to 3Cu^{2+} + 2NO + 4H_2O\)
\(n_{Cu} = 0,12(mol)\)
Theo PTHH :
0,5a + \(\dfrac{3}{8}\)(0,88 - 2b -4c) = 0,12(3)
(1)(2)(3) suy ra a = 0,216 ; b = 0,024 ; c = 0,2
Suy ra V = 0,2.22,4 = 4,48(lít).Đáp án B

Chọn A
Cách 1:
Giả thiết hỗn hợp ban đầu được tạo ra từ a mol Fe và b mol O 2
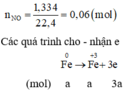

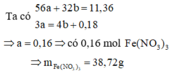
Cách 2:
Quy đổi hỗn hợp về Fe (x mol) và O (y mol)
→ 56x + 16y = 11,36 mol (1)
Bảo toàn e: 3nFe = 2nO + 3 nNO
→ 3x – 2y = 0,18 (2)
Từ (1)(2) → x = 0,16; y = 0,15
Số mol NO3- = ne cho = 3 nFe = 0,48 mol
mmuối = mFe + mNO3- = 0,16.56 + 0,48.62 = 38,72g

n O = 39,2.18,367%/16 = 0,45(mol)
Bảo toàn e :
n SO4 2-(trong muối) = n e cho = 2n O + 2n SO2 = 0,45.2 + 0,4.2 = 1,7(mol)
Bảo toàn nguyên tố với S :
n H2SO4 pư = n SO4 2-(trong muối) + n SO2 = 1,7 + 0,4 = 2,1(mol)
=> n H2SO4 đã dùng = 2,1/(100% -20%) = 2,625(mol)
=> a = CM H2SO4 = 2,625/2,5 = 1,05(M)

Coi hh gồm Fe và O.
Ta có: 56nFe + 16nO = 14,64 (1)
Ta có: \(n_{NO}=\dfrac{1,4874}{24,79}=0,06\left(mol\right)\)
Theo ĐLBT e, có: 3nFe = 2nO + 3nNO ⇒ 3nFe - 2nO = 0,06.3 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,201\left(mol\right)\\n_O=0,2115\left(mol\right)\end{matrix}\right.\)
⇒ m = mFe = 0,201.56 = 11,256 (g)

a, Ta có: $n_{O}=0,6(mol)$
Suy ra $n_{H^+/pu}=1,2(mol)\Rightarrow n_{H_2SO_4}=0,6(mol)$
Bảo toàn khối lượng ta có: $m_{muoi}=29,6+0,6.96=87,2(g)$

- Từ quá trình phản ứng ta thấy số oxi hoá của các chất phản ứng ở trạng thái đầu là
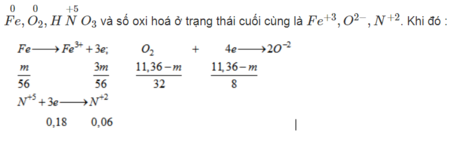
Áp dụng ĐLBT electron ta có:
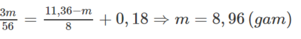

m=10,08 gam
Giải thích các bước giải:
Sơ đồ phản ứng:
X+HCl→muối+H2+H2OX+HCl→muối+H2+H2O
Ta có: nHCl=0,3.1=0,3 mol; nH2=0,67222,4=0,03 molnHCl=0,3.1=0,3 mol; nH2=0,67222,4=0,03 mol
Bảo toàn nguyên tố H:
nHCl=2nH2+2nH2O→nH2O=0,3−0,03.22=0,12
Sơ đồ phản ứng:
\(X+HCl\rightarrow muoi+H_2+H_2O\)
Ta có:
\(n_{HCl}=0,3.1=0,3\left(mol\right)\)
\(n_{H2}=\frac{0,672}{22,4}=0,03\left(mol\right)\)
Bảo toàn nguyên tố H:
\(n_{HCl}=2n_{H2}+2n_{H2O}\Rightarrow n_{H2O}=\frac{0,3-0,03.2}{2}=0,12\left(mol\right)\)
Bảo toàn O:
\(n_{O.trong.X}=n_{H2O}=0,12\left(mol\right)\)
\(\Rightarrow m_{Fe.trong,X}=m=m_X-m_O=12-0,12.16=10,08\left(g\right)\)




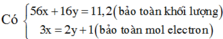
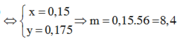
bạn để link như vậy thì khó tìm lắm mk làm cách khác đc ko
\(Fe+\left[O\right]\rightarrow A\)
\(A+HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+H_2O\)
\(n_{NO}=0.025\left(mol\right)\)
BTKL ta có: \(56n_{Fe}+16n_O=3\)
BT(e) ta có: \(3n_{Fe}-2n_O=3n_{NO}=0.075\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0.045\left(mol\right)\\n_O=0.03\left(mol\right)\end{matrix}\right.\)
\(n_{Fe\left(NO_3\right)_3}=n_{Fe}=0.045\left(mol\right)\)
Do HNO3 vừa đủ nên \(n_{HNO_3}=0.045\cdot3+0.025=0.16\)
CM(HNO3)=\(\frac{0.16}{0.2}=0.8\left(M\right)\)