Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Nhiệt phân:
NaNO3→NaNO2+0,5O2(1)
0,05 ← 0,025
2Al(NO3)3→Al2O3+6NO2+1,5O2(2)
Cu(NO3)2→CuO+2NO2+0,5O2(3)
2NO2+0,5O2+H2O→2HNO3
x → 0,25x → x
nO2 dư=0,56/22,4=0,025=nO2(1)
C%HNO3=63x/(46x+0,25x.32+112,5)=0,125=> x=0,25 mol
=> nNO2=0,25 mol; nO2=nO2(2)+nO2(3)+nO2(1)=0,25x+0,025=0,0875 mol
BTKL: mX=mY+mNO2+mO2=10+0,25.46+0,0875.32=24,3 gam
%mNaNO3=0,05.85/24,3=17,49%

Đáp án B
Các phản ứng xảy ra:

Do đó khí còn lại thoát ra là lượng khí O2 sinh ra do phản ứng nhiệt phân NaNO3.
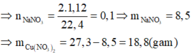

Đáp án C
Đặt số mol Fe là a , Mg là 2a , Na là b
Bảo toàn N : 2nFe(NO3)2 + 2nMg(NO3)2 = nHNO3
<=>6a = 1,2.0,1
<=> a=0,02
2NaNO3 ➝ 2NaNO2 + O2
b ➝ \(\dfrac{b}{2}\)
2Mg(NO3)2 ➝ 2MgO + 4NO2 +O2
0,04 ➝ 0,02
2Fe(NO3)2 ➝ 2FeO + 4NO2 + O2
0,02 ➝ 0,01
4FeO + O2 ➝ 2Fe2O3
0,02 ➝ 0,005
2H2O + 4NO2 + O2 ➝ 4HNO3
0,03 ← 0,12
=> 0,01 + 0,02 - 0,005 + \(\dfrac{b}{2}\) = 0,03
<=> b= 0,01
=> m = 0,01.85 + 0,02.180 + 0,04.148=10,37

$n_{O_2} = 0,05(mol)$
4NO2 + O2 + 2H2O → 4HNO3
4a...........a..........................4a.............(mol)
Suy ra : $n_{NO_2} = 4a(mol) ; n_{O_2} = 0,05 + a(mol)$
Gọi $n_{NaNO_3} = b(mol) ; n_{Cu(NO_3)_2} = c \Rightarrow 85b + 188c= 27,3(1)$
$2NaNO_3 \xrightarrow{t^o} 2NaNO_2 + O_2$
$2Cu(NO_3)_2 \xrightarrow{t^o} 2CuO + 4NO_2 + O_2$
Theo PTHH :
$n_{O_2} = 0,5b + 0,5c = 0,05 + a(2)$
$n_{NO_2} = 2b = 4a(3)$
Từ (1)(2)(3) suy ra a = 0,05 ; b = 0,1 ; c = 0,1
Suy ra:
$n_{HNO_3} = 4a = 0,2(mol)$
$[H^+] = \dfrac{0,2}{2} = 0,1M$
$pH = -log(0,1) = 1$

NaNO3➞NaNO2 +\(\dfrac{1}{2}\)O2
Cu(NO3)2 ➞CuO +2NO2 +\(\dfrac{1}{2}O2\)
2NO2 +\(\dfrac{1}{2}O2+H2O\rightarrow2HNO3\)
Do đó khí còn lại thoát ra là lượng khí O2 sinh ra do pứ nhiệt phân NaNo3
nNaNO3=\(\dfrac{2.1,12}{22,4}=0.1\Rightarrow m_{NaNO3}=0.1.85=8,5\)
mCu(NO3)2 = 27,3 - 8,5 =18,8 (g)

Phần O2 sinh ra khi nung đi hết vào kim loại tạo oxit, đó là lý do ta chỉ thu được một khí Z là NO2 (0,4 mol).
Khi nung hỗn hợp T trong không khí thì sản phẩm thu được sẽ gồm các oxit “bão hòa” hóa trị (CuO, Fe2O3).
Số mol electron tối đa mà X có thể cho là: 3nNO =0,54 mol
Như vậy sẽ cần 0,54/2 = 0,27 mol O đưa vào rắn X để thu được 41,6 gam rắn gồm các oxit “bão hòa”.
→mX = mr + mO = 41,6 -0,27.16=37,28 gam
→m =mX = mNO2 = 37,28+46x0,4=55,68 gam
Chọn đáp án A

2NaNO3 → 2NaNO2 + O2
a a a/2
| 2Zn(NO3)2 |
→ |
2ZnO |
+ |
4NO2 |
+ |
O2 |
b b 2b b/2
4NO2 + O2 + 2H2O → 4HNO3
2b → b/2 2b
⇒ n khí bay ra là O2 n = a/2 = 0,15
⇒ a = 0,3
nY = 0,4 ⇒ a/2 + 5b/2 =0,4 ⇒ b = 0,1
⇒ nH+/Z = 2b = 0,2 ⇒ [H+] = 0,2 : 2 = 0,1M
⇒pH = 1
Đáp án C.
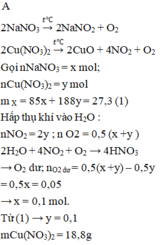

2NaNO3 → 2NaNO2 + O2
a a a/2
2Cu(NO3)2
→
2CuO
+
4NO2
+
O2
b b 2b b/2
4NO2 + O2 + 2H2O → 4HNO3
2b → b/2
⇒ n khí bay ra là O2 dư với số mol a/2 = 0,05 mol
⇒ a = 0,1
m Cu(NO3)2 + m NaNO3 =27,3
⇒ 188.b + 85a = 27,3 ⇒ b = 0,1 mol
m Cu(NO3)2 = 18,8
Đáp án A.