Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Axit formic là axit yếu. Tuy nhiên nó mạnh nhất trong dãy đồng đẳng của axit cacboxylic no, đơn chức, mạch hở và mạnh hơn axit cacbonic:(H2CO3) do hiệu ứng dồn mật độ electron trong nhóm
-COOH. Axit cacboxylic không có phản ứng tráng bạc nhưng riêng HCOOH thì có.
Phương trình phản ứng như sau:
HCOOH + 2[Ag(NH3)2]OH → (NH4)2CO3 + 2Ag↓ + 2NH3↑ + H2O

a) C2H4 + O2 -> CH3CHO
Hỗn hợp khí X gồm C2H4 chưa phản ứng và CH3CHO. Khi X tác dụng với dung dịch AgNO3/NH3
CH3CHO + 2AgNO3 + 3NH3 + H2O -> CH3COONH4 + 2Ag + 2NH4NO3
Số mol Ag = 0,150 mol. Vậy số mol CH3CHO = 0,0750 mol
Hiệu suất của quá trình oxi hóa etilen :  .100% = 75%
.100% = 75%

- Dung dịch bị vẩn đục là do phản ứng tạo ra phenol.
- Nhận xét về tính axit của phenol: Phenol có tính axit yếu hơn nấc thứ nhất của axit cacbonic H2CO3, nên bị axit cacbonic đẩy ra khỏi dung dịch muối.

- X là anđehit đơn chức
RCHO + 2AgNO3 + 3NH3 + H2O → RCOONH4 + 2Ag + 2NH4NO3
nAg = 0.02 mol => nRCHO = \(\dfrac{1}{2}\) nAg = 0,01 mol
MRCHO = 58,0 g/mol. R là C2H5 , X là CH3CH2CHO.
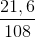 = 0,2 (mol)
= 0,2 (mol)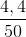 . 100% = 8,8%
. 100% = 8,8%
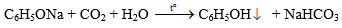
CaCO3 t∘→→t∘ CaO+CO2
nCO2nCO2 = nCaCO3nCaCO3 = 52,65/100 = 0,5265 (mol)
Vì phản ứng trên có h = 95 % nên nCO2nCO2 thực tế thu được:
nCO2nCO2 = 0,5265 * 95/100 = 0,5 mol
Ta có nNaOH = 0,5000 x 1,800 = 0,900 (mol)
Tỉ lệ số mol giữa NaOH và CO2 : 1 < nNaOHnCO2nNaOHnCO2 = 0,90000,50020,90000,5002 < 2
Do đó, phản ứng tạo thành hỗn hợp hai muối: NaHCO3 và Na2CO3
CO2 + 2NaOH → Na2CO3 + H2O
0,4500 mol 0,9000 mol 0,4500 mol
Na2CO3 + CO2 + H2O → 2NaHCO3
0,05020 mol 0,05020 mol 0,1004 mol
Từ đó tính ra được khối lượng NaHCO3 là 8,434 g và khối lượng của Na2CO3 là 42,38 g