Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi x là thành phần phần trăm của \(_{17}^{35}Cl\)
Ta có: \(\overline{A}=\frac{35x+37\left(100-x\right)}{100}=35,5\leftrightarrow x=75\)
Vậy trong tự nhiên đồng vị \(_{17}^{35}Cl\) chiếm 75% và \(_{17}^{37}Cl\) chiếm 25%
b) Ta có \(\%Cl=\frac{35,5\cdot100}{39+35,5+16\cdot4}=\frac{7100}{277}\sim25,63\%\)
\(\Rightarrow\%^{35}Cl=\frac{25,63\cdot75}{100}=\frac{7689}{400}\sim19,22\%\)

TÍNH :
a, \(Fe_2O_3=56.2+16.3=160đvc\)
b, \(Fe_2\left(SO_4\right)_3=56.2+\left(32+16.4\right).3=400đvc\)
c, \(C_6H_{12}O_6=12.6+1.12+16.6=180đvc\)
d, \(Al\left(OH\right)_3=27+\left(16+1\right).3=78đvc\)
e, \(FeCl_3=56+35,5.3=162,5đvc\)
MÌNH LÀM SONG RỒI CHÚC BẠN MAY MẮN
TÍNH PHÂN TỬ KHỐI CỦA CÁC NGUYÊN TỐ :
a) PTK của \(Fe_2O_3=56.2+16.3=160\left(\text{đ}vc\right)\)
b) PTK của \(Fe_2\left(SO4\right)_3=56.2+3\left(32+16.4\right)=400\left(\text{đ}vc\right)\)
c) PTK của \(C_6H_{12}O_6=6.12+12.1+6.16=180\left(\text{đ}vc\right)\)
d) PTK của \(Al\left(OH\right)_3=27+3\left(1+16\right)=78\left(\text{đ}vc\right)\)
e) PTK của \(FeCl3=56+3.35,5=162,5\left(\text{đ}vc\right)\)

1) 3M+4nHNO3→3M(NO3)n+nNO+2nH2O
M+HNO3→M(NO3)n+NO+H2OM0 → M+n + ne |3
N+5 + 3e → N+2 | n
Tương tự:
2) 2M+2nH2SO4→M2(SO4)n+nSO2+2nH2OM+H2SO4→M2(SO4)n+SO2+H2O
3) 8M+30HNO3→8M(NO3)3+3N2O+15H2O
M0 + 3e → M+3 | 8
2N+5 + 8e → N2+1O | 3M+HNO3→M(NO3)3+N2O+H2O Ư
4) 2FexOy+2yH2SO4→xFe2...

1.
a) Gọi p là số proton của nguyên tố X
Đồng vị X1 có 3 loại hạt bằng nhau nên 3p = 18 suy ra p = 6
Đồng vị X2 có tổng số hạt 20 nên 2p + n’ = 20 suy ra n’ = 8
Số khối của các đồng vị X1, X2 lần lượt là 12, 14
Phần trăm hai đồng vị bằng nhau suy ra mỗi đồng vị chiếm 50%
Atb = (12.50 + 14.50) / 100 = 13 đvC
b)
Gọi số khối của hai đồng vị X, Y là A1 và A2; phần trăm số nguyên tử của hai đồng vị này là x1 và x2. Theo giả thiết ta có:
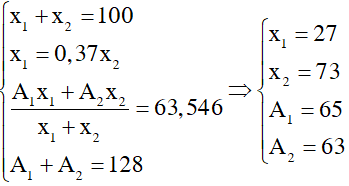
1
a , các loại hạt trong X1 bằng nhau <=> p=n1=e=6 (hạt) => A1 = 12
=> n2 = 20-6.12=8(hạt) => A2 = 8+6=14
%X1 = %X2 = 50%
\(\overline{\text{A}}=\frac{14.50+12.50}{100}=13\)
2 , gọi 2 đồng vị A1p Y và A2p Z , phần trăm của 2 đồng vị lần lượt la x1 , x2
Theo bài ra
A1 + A2 =128
x1 + x2 = 100
\(\overline{M}=\frac{A_1x_1+A_2x_2}{100}=\) 63,54
x1 - 0,37x2 = 0
=> A1 = 65 , A2 = 63


\(\overline{A_N}=\dfrac{14.99,63+15.0,37}{100}\approx14,003\)
Xét 1 mol NaNO3
\(n_{NaNO_3}=\dfrac{1,700074}{85,003}\approx0,02\left(mol\right)\)
=> \(n_N=n_{NaNO_3}=0,02\)
Số nguyên tử N có trong NaNO3:
0,02.6,02.1023 = 1204.1019 (nguyen tư)
Số nguyên tử 14N : 99,63%.1204.1019
\(\approx1,1995.10^{22}\) (ngtu)