
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Y chứa H2 → Z không chứa NO3-. Lập sơ đồ phản ứng:
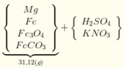
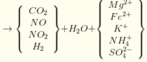
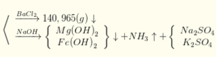
n(H2SO4) =n(SO42-) = n(BaSO4) = 0,605 mol; n(NH4+) = n(khí) = 0,025 mol
Áp dụng ĐLBT điện tích: n(Na+) + n(K+/Z) = 2n(SO42-)
→ n(KNO3) = n(K+) = 0,605*2 – 1,085 = 0,125 mol → (b) sai
Đặt n(Mg2+) = x; n(Fe2+) = y
→ (1) n(NaOH) = 2x + 2y + 0,025 = 1,085 mol
(2) m(kết tủa) = 58x + 90y = 42,9 gam
Giải (1) và (2): x = 0,15 mol; y = 0,38 mol → (e) đúng.
→ m = 0,15*24 + 0,38*56 + 0,125*39 + 0,025*18 + 0,605*96 = 88,285 gam → (a) sai
Áp dụng ĐLBT khối lượng: m(H2O) = 31,12 + 0,605*98 + 0,125*101 – 88,285 – 0,2*29,2 = 8,91
→ n(H2O) = 0,495 mol.
Áp dụng ĐLBT nguyên tố Hiđro: n(H2) = (0,605*2 – 0,025*4 – 0,495*2)/2 = 0,06 mol
Áp dụng ĐLBT nguyên tố Nitơ: Tổng n(NO, NO2) = tổng n(N/Y) = 0,125 – 0,025 = 0,1 mol
→ n(FeCO3) = n(CO2)= 0,2 – 0,1 – 0,06 = 0,04 mol; → %m(FeCO3) = 14,91% → (c) sai
m(X) = m(Mg) + m(Fe) + m(O) + m(CO32-) → m(O) = 31,12 – 0,15*24 -0,38*56 – 0,04*60 = 3,84
→ n(O) = 0,24 mol → n(Fe3O4) = 0,06 mol → (d) sai
Các kết luận không đúng là: (a); (b); (c); (d) → Đáp án D.

Chọn đáp án D
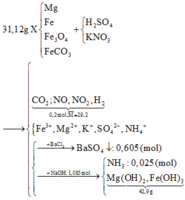
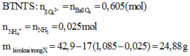
Quy đổi hỗn hợp X thành Fe, Mg, O và CO2
Đặt a, b là số mol của O và CO2 trong X. Đặt x là số mol H2
∑ m(O +CO2) = 31,12 – 24,88 = 6,24 (1)
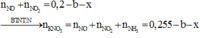
Sau phản ứng với dung dịch NaOH thu được dd chứa K2SO4 và Na2SO4
Bảo toàn điện tích:
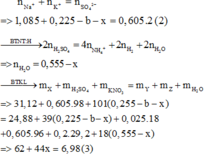
Từ (1), (2) và (3)
=> a = 0,28 (mol) ; b = 0,04 (mol) ; x = 0,06 (mol
=> m = 24,88 + 39 ( 0,255 –b –x) + 0,025.18 + 0,605.96 = 88, 285 => nhận định a) sai
nKNO3 = 0,225 – b – x = 0,125 => nhận định b) sai
%FeCO3 = ( 0,04.116/ 31,12).100% = 14,91% => nhận định c) sai
nO = 4nFe3O4 + nFeCO3 => nFe3O4 = 0,06 => nhận định d) sai
=> có tất cả 4 nhận định sai.

Đáp án A
Hòa tan hết 7,44 gam hỗn hợp rắn vào 0,4 mol HCl và 0,05 mol NaNO3 thu được 22,47 gam muối và 0,02 mol hỗn hợp khí gồm NO và N2.
Giải được số mol NO và N2 đều là 0,01 mol.
Do X chứa muối nên HCl phản ứng hết.
BTKL: m H 2 O = 7 , 44 + 0 , 4 . 36 , 5 + 0 , 05 . 85 - 22 , 47 - 0 , 02 . 29 = 3 , 24 → n H 2 O = 0 , 18
BTNT H: n N H 4 + = 0 , 4 - 0 , 18 . 2 4 = 0 , 01 m o l
Cho NaOH dư vào X thu được kết tủa Y, nung Y trong không khí thu được rắn chứa MgO và Fe2O3 có khối lượng 9,6 gam.
Lượng O để oxi hóa hỗn hợp ban đầu lên tối đa là: n O = 9 , 6 - 7 , 44 16 = 0 , 135 m o l
Cho AgNO3 dư tác dụng với dung dịch X ta thu được kết tủa gồm AgCl 0,4 mol (bảo toàn C) và Ag.
Bảo toàn e:
n A g = 0 , 135 . 2 - 0 , 01 . 8 - 0 , 01 . 3 - 0 , 01 . 10 = 0 , 06 m o l → m = 63 , 88 g a m