Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Fe + CuSO4 => FeSO4 + Cu
mCu =mFe tăng = 50.4% = 2(g) => nCu = 0,03125 mol
=> nFeSO4 = nCu = 0,03125
CM FeSO4 = 0,03125/0,5 = 0,0625(M)
sai rồi nha đồ ngu
dễ thế mà sai ahihi![]()
mFe tăng=mCu bám vào - mFe tan ra nhé đồ ngáo

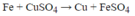
Theo phương trình cứ 56 gam Fe tan vào dung dịch thì có 64 gam Cu tách ra khỏi dung dịch. Thanh Fe tăng khối lượng nên khối lượng dung dịch phải giảm đi đúng bằng khối lượng thanh Fe tăng lên.
Vậy khối lượng thanh sắt tăng 0,8 gam khối lượng dung dịch giảm so với ban đầu 0,8 gam

nAgNO3= 0,1 (mol)
Al + 3AgNO3 \(\rightarrow\) Al(NO3)3 + 3Ag
Cứ 1 mol Al pư thì khối lượng thanh Al tăng 297 g
0,01 mol <--------------------------------------- (52,97 - 50)
a) mAl pư = 0,01 . 27=,27 (g)
Theo pt nAg = 3nAl=3 . 0,01 = 0,03 (mol) = nAgNO3 pư
mAg=0,03 . 108 = 3,24 (g)
b)nAgNO3 dư = 0,1 - 0,03 = 0,07 (mol)
CM (AgNO3)= \(\frac{0,07}{0,25}\) = 0,28 (M)
CM (Al(NO3)3) = \(\frac{0,01}{0,25}\) = 0,04 (M)

Gọi số mol FeSO4 là x
→ Số mol ZnSO4 là 2,5x
Fe + CuSO4 → FeSO4 + Cu↓
x → x → x → x
Zn + CuSO4 → ZnSO4 + Zn↓
2,5x → 2,5x → 2,5x → 2,5x
m dung dịch giảm = mCu - mFe + mZn
→ (x + 2,5x).64 - 56x + 65.2,5x = 0,22
→ x = 0,04
nCu = 0,04 . (1+2,5) = 0,14 (mol)
mCu = 0,14 . 64 = 8,96g
nCuSO4 p.ư = 0,04 + 2,5 . 0,04 = 0,14 mol
Sau phản ứng dung dịch gồm: FeSO4 (0,04 mol); ZnSO4 (0,1 mol), CuSO4 dư (a mol)
Cho dung dịch tác dụng với NaOH dư:
FeSO4 + 2NaOH → Na2SO4 + Fe(OH)2↓
0,04 → 0,04
ZnSO4 + 4NaOH → Na2ZnO2 + Na2SO4 + 2H2O
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2↓
a → a
Nung kết tủa đến khối lượng không đổi:
4Fe(OH)2 + O2 -to→ 2Fe2O3 + 4H2O
0,04 → 0,02
Cu(OH)2 -to→ CuO + H2O
a → a
mcr = mFe2O3 + mCuO
→ 0,02 . 160 + a.80 = 14,5
→ a = 0,14125
nCuSO4 = nCuSO4 p.ư + nCuSO4 dư = 0,14 + 0,14125 = 0,28125 mol
CM (CuSO4) = 0,28125 : 0,5 = 0,5625M


a, PT: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
Gọi nFe (pư) = x (mol) ⇒ nCu = nFe = x (mol)
Ta có: m tăng = mCu - mFe (pư)
⇒ 1,2 = 64x - 56x ⇒ x = 0,15 (mol)
⇒ mCu = 0,15.64 = 9,6 (g)
b, Ta có: \(m_{CuSO_4}=400.10\%=40\left(g\right)\Rightarrow n_{CuSO_4}=\dfrac{40}{160}=0,25\left(mol\right)\)
Theo PT: \(n_{FeSO_4}=n_{CuSO_4\left(pư\right)}=n_{Fe}=n_{Cu}=0,15\left(mol\right)\)
⇒ nCuSO4 (dư) = 0,25 - 0,15 = 0,1 (mol)
Có: m dd sau pư = mFe + m dd CuSO4 - mCu = 0,15.56 + 400 - 9,6 = 398,8 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,15.152}{398,8}.100\%\approx5,72\%\\C\%_{CuSO_4\left(dư\right)}=\dfrac{0,1.160}{398,8}.100\%\approx4,01\%\end{matrix}\right.\)
Hay Đó