Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C.
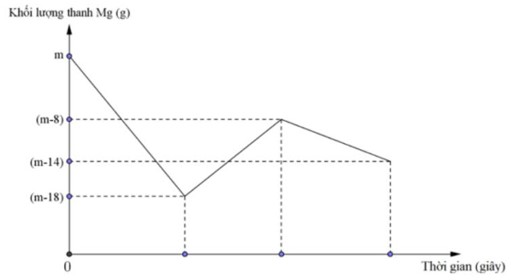
Tại thời điểm t1: thanh Mg giảm 18 gam do Mg tác dụng với H+ và NO3–
3Mg + 8H+ + 2NO3– → 3Mg2+ + 2NO + 4H2O (1)
mol: 0,75 → 2 0,5
Tại thời điểm t1 đến t2: thanh Mg tăng 10 gam do Mg đã phản ứng với Cu2+
Mg + Cu2+ → Mg2+ + Cu (2)
Ta có Dmtăng = (64 – 24).a = 10 Þ a = 0,25 mol
Tại thời điểm t2 đến t3: thanh Mg giảm 6 gam do Mg đã phản ứng với H+
Mg + 2H+ → Mg2+ + H2 (3)
Ta có mgiảm = mMg = 6 Þ nMg = 0,25 mol → 2 + 3 b = 2 + 0,5 = 2,5 mol. Vậy a : b = 1 : 10

Đáp án D
Dựa vào đồ thị thấy tại thời điểm m-18 gam thì Mg phản ứng hết H+ và NO3- sinh ra Mg2+ và NO
Khi đó toàn bộ lượng NO3- chuyển hóa hết thành NO : 2a mol
Có nMg phản ứng = 18 : 24 = 0,75 mol
Bảo toàn electron → 0,75.2 = 2a. 3 → a = 0,25 mol
→ nH+ pư = 0,25. 8 = 2 mol → nH+ dư : b- 2 mol
Tại thời điểm m- 8 thì Mg phản ứng với Cu2+ sinh ra Cu
Tại thời điểm m- 14 thì Mg tiếp tục phản ứng với HCl dư sinh khí H2
Bảo toàn electron
![]()
Khi đó 14= 24. 0,5b - 0,25. 64 → b= 2,5
a : b= 0,25 : 2,5 = 1: 10.

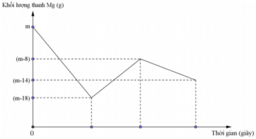
Dựa vào đồ thị:
Đoạn 1: khối lượng thạnh Mg giảm 18 gam do
3Mg + 8H+ + 2NO3-
→
3Mg2+ + 2NO + 4H2O
0,75 → 2 → 0,5
Đoạn 2: khối lượng thanh Mg tăng 10 gam do
Mg + Cu2+
→
Mg2+ + Cu
a ← a → a
64a – 24a = 10 ⇒ a = 0,25
Đoạn 3: Khối lượng thanh Mg giảm 6 gam do
Mg + 2H+
→
Mg2+ + H2
0,25 → 0,5
⇒ b = nH+ = 2 + 0,5 = 2,5 ⇒ a : b = 0,25 : 2,5 = 1 : 10 ⇒ Chọn C.

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

Bạn bấn vào đây, có người hỏi bài này rồi nhá Câu hỏi của Mạc Nhược Ca - Hóa học lớp 12 | Học trực tuyến

nCu = 0,02; nAg = 0,005 → Tổng số mol e cho tối đa: = 0,02.2 + 0,005.1 = 0,45
nH+ = 0,09; nNO3- = 0,06 (dư)
4H+ + NO3- + 3e → NO + 2H2O
0,06 0,045 0,015
Cu, Ag đã phản ứng hết
2NO + O2 → 2NO2
0,015 0,0075 0,015
4NO2 + O2 + 2H2O → 4HNO3
0,015 0,015
Nồng độ mol HNO3 = 0,015:0,15 = 0,1 → pH = 1

 với các chất sau:
với các chất sau:
Đáp án C.
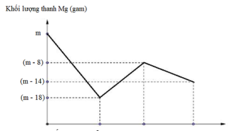
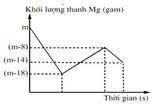
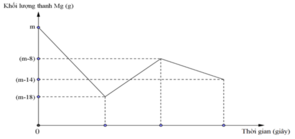
Phân tích đồ thị:
+ Đoạn 1: 3Mg + 8H+ + 2NO3- → 3Mg2+ + 2NO + 4H2O.
+ Đoạn 2: Mg + Cu2+ → Mg2+ + Cu
+ Đoạn 3: Mg + 2H+ → Mg2+ + H2