Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
Cho 3 chất vào H2O
- Tan là BaO
- Không tan là MgO và CuO
Cho CO đi qua 2 chất còn lại nung nóng
- Có chất rắn màu đỏ là CuO
- Còn lại là MgO
b)
Cho 3 chất vào dd HCl
- Tan và có khí thoát ra là Al
- Tan và tạo dd màu xanh làm là CuO
- Tan và tạo dd không màu là MgO
- Không tan là Ag
c)
Cho 4 chất vào nước sau đó cho quỳ tím vào
- Tan và làm quỳ tím hóa đỏ là P2O5
- Tan và làm quỳ tím hóa xanh là CaO và Na2O
- Không tan là MgO
Cho CO2 vào 2 dd tạo thành của CaO và Na2O
- Có kết tủa là CaO
- Còn lại là Na2O
d)
Cho 4 chất vào nước sau đó cho quỳ tím vào
- Tan và quỳ tím hóa đỏ là P2O5
- Tan và làm quỳ tím hóa xanh là Na2CO3
- Tan và quỳ tím không đổi màu là NaCl
- Không tan là MgCO3
Trích mẫu thử :
a) * Cho nước vào 3 ống nghiệm
+Tan :BaO
+Không tan :MgO, CuO
* Tiếp theo cho dung dịch HCl vào , lắc nhẹ xong cho thêm dung dịch NaOH :
+Xuất hiện ↓ xanh : CuO
+Xuất hiện ↓ trắng :MgO
b)* Cho dung dịch NaOH vào 4 ống nghiệm
+Ống nghiệm nào tan :Al
+Các ống nghiệm không tan : CuO ,MgO ,Ag
*Tiếp theo cho dung dịch HCl vào , lắc nhẹ xong cho thêm dung dịch NaOH :
+Xuất hiện ↓ xanh : CuO
+Xuất hiện ↓ trắng :MgO
+Không hiện tượng : Ag

Đáp án D
Trong dãy oxit:
Oxit có liên kết ion là Na2O, CaO.
Oxit có liên kết cộng hóa trị phân cực là SiO2, P2O5, SO3.

Liên kết trong các oxit đó là liên kết giữa oxi và các nguyên tố thuộc chu kì 3.
Căn cứ vào hiệu độ âm điện, có thể dự đoán liên kết trong các oxit : Na 2 O , MgO, Al 2 O 3 là liên kết ion, liên kết trong các oxit : SiO 2 , P 2 O 5 , SO 2 là các liên kết cộng hoá trị có cực, liên kết trong oxit Cl 2 O 7 là liên kết cộng hoá trị không cực

Oxit bazơ: Na2O, MgO (2)
Oxit lưỡng tính: Al2O3 (1)
Oxit axit: SiO2, P2O5, SO3, Cl2O7 (3)

1. Cho các oxit sau : CaO , Fe2O3 , SO3, SiO2, P2O5 . Dãy các oxit axit là:
A. CaO , P2O5 , SO3
B. CaO,Fe2O3,CuO
C. CaO, SO3 , SiO2
D. SO3, P2O5,SiO2,MnO2
Theo e nghĩ thì không có nhóm nào là oxit axit cả.
Chỗ câu D á Trên đề ko cs MnO2 mà sao tự nhiên chỗ câu D nó lại có.
Câu D nếu nó bỏ đi MnO2 thì câu D là dãy các Oxit axit.

Đáp án C
Mg, Al, Si. P cùng nằm trong một chu kì, độ âm điện tăng dần MG < Al <Si < P
∆X = XO- X nguyên tố, độ âm điện của nguyên tố càng nhỏ nguyên tố càng phân cực.

a)
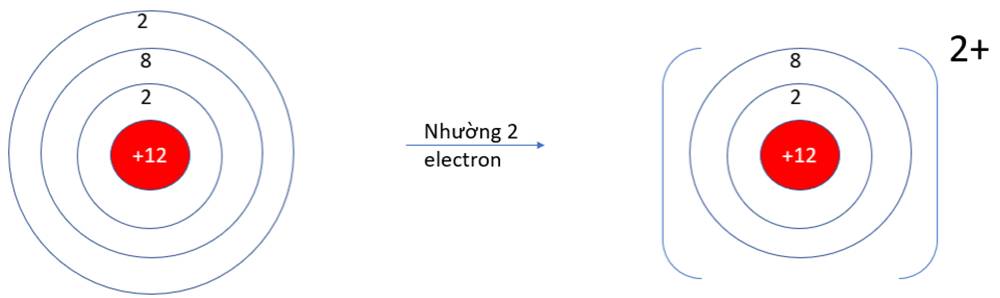
- Ở dạng nguyên tử, Na và Mg đều có 3 lớp electron. Ở dạng ion Na+, Mg2+ chỉ có 2 lớp electron
=> Bán kính nguyên tử Na, Mg lớn hơn bán kính các ion kim loại tương ứng
b, Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử O nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2O.
2Na+ + O2- → Na2O
Vì Na2O là hợp chất ion nên ở điều kiện thường Na2O tồn tại ở thể rắn.
Nguyên tử Mg nhường 2 electron, nguyên tử O nhận 2 electron từ nguyên tử Mg để hình thành hợp chất ion MgO.
Mg2+ + O2- → MgO
Vì MgO là hợp chất ion nên ở điều kiện thường MgO tồn tại ở thể rắn.
c, Tá có:
+ Bán kính ion Na+ < bán kính ion Mg2+.
+ Điện tích ion Mg2+ < điện tích ion Na+.
Vậy nhiệt độ nóng chảy của MgO (2852oC) cao hơn rất nhiều so với Na2O (1132oC) do năng lượng phân li tỉ lệ thuận với điện tích ion và tỉ lệ nghịch với bán kính ion.

Hiệu độ âm điện của các chất:
Na2O: 2,51 liên kết ion.
MgO: 2,13 liên kết ion.
Al2O3: 1,83 liên kết ion.
SiO2: 1,54 liên kết cộng hóa trị có cực
P2O5: 1,25 liên kết cộng hóa trị có cực
SO3: 0,86 liên kết cộng hóa trị có cực
Cl2O7: 0,28 liên kết cộng hóa trị không cực
+ Trích thành các mẫu thử nhỏ, đánh số:
+ Cho H2O lần lượt vào
. . . ..Tan ra là CaO, P2O5 và BaO
\(CaO + H2O ---> Ca(OH)2 \)
\(P_2O_5 + 3H_2O---> 2H_3PO_4 \)
\(BaO + H_2O ---> Ba(OH)_2\)
. . . Không tan là Mg, MgO và SiO2
+ Cho quỳ tím vào các chất tan ra ở trên.
. . . chất nào làm quỳ tím hóa đỏ là H3PO4 --> Chất ban đầu là P2O5.
. . . . Chất làm quỳ tím hóa xanh là Ca(OH)2 và Ba(OH)2 . Thổi CO2 vào, mẫu thử nào thấy có kết tủa trắng là Ca(OH)2 --> Chất ban đầu là Cao. chất còn lại không có hiện tượng gì là Ba(OH)2 --> Chất ban đầu là BaO
\(CO_2 + Ca(OH)2 ---> CaCO_3 + H_2O\)
+ Cho dung dich axit sunfuric lần lượt vào các chất không tan trong nước, quan sat:
. . . . Mẫu thử nào không có hiện tượng (không tan) là SiO2
. . . .Mẫu thử nào tan ra có xuất hiện bọt khí là Mg
\(Mg + H_2SO_4 ---> MgSO_4 + H_2\)
. . . . . Mẫu thử nào tan ra là MgO
\(MgO + H_2SO_4 ---> MgSO_4 + H_2O\)
Màu xám ko phải màu xanh, nhầm