Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt x nguyên tử khối của đồng vị còn lại
Ta có : \(\overline{M}=\dfrac{54,5.79+\left(100-54,5\right).x}{100}=79,91\)
\(\rightarrow x=81\)
Vậy nguyên tử khối của đồng vị còn lại : \(^{81}X\)

Chọn C
- Phần trăm của đồng vị còn lại là 100% - 54,5% = 45,5%
- Công thức tính nguyên tử khối trung bình:
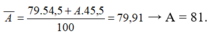

\(\overline{NTK}_{Br}=79,55\\ \Leftrightarrow\dfrac{79.55\%+A_2.45\%}{100\%}=79,55\\ \Leftrightarrow A_2\approx80,22\left(đ.v.C\right)\)

\(a.Đặt:\%^{79}Br=a\left(a>0\right)\\ \Rightarrow \%^{81}Br=100\%-a\\ \overline{NTK}_{Br}=79,91\\ \Leftrightarrow79a+81.\left(100\%-a\right)=79,91\\ \Leftrightarrow a=54,5\%\\ \Rightarrow\%^{79}Br=54,5\%;\%^{81}Br=45,5\%\)
b. Phần trăm theo KL đồng vị 79Br trong phân tử CaBr2:
\(54,5\%.\dfrac{70.91.2}{79,91.2+40}\approx43,59\%\)
c.
\(\left\{{}\begin{matrix}P=E\\P+N=79\\\left(P+E\right)-N=26\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P+N=79\\2P-N=26\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=35\\N=44\end{matrix}\right.\)

Ta có: \(\overline{M_{Br}}=\dfrac{79\cdot x+81\cdot y}{100}=79,91\)
Mà \(x+y=100\)
\(\Rightarrow\left\{{}\begin{matrix}\%^{79}Br=x=54,5\%\\\%^{81}Br=y=45,5\%\end{matrix}\right.\)
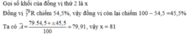
Cấu hình electron theo thứ tự mức năng lượng
1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 4p^6 3d^9
Cấu hình electron theo thứ tự lớp
1s^2 2s^2 2p^6 3s^2 3p^6 3d^9 4s^2 4p^6
Gọi A là số khối của đồng vị 2
Ta có :
79,91 = [79*54,5%+A*45,5%]/100%
<=> A = 81
3d\(^9\) cơ à