
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Y2+ có : số hạt mang điện là [p + (e – 2)]
=> [p + (e – 2)] – n = 10
=> 2p – n = 12
Y2+ có 34 hạt cơ bản => Y có 34 + 2 = 36 hạt cơ bản
=> p + e + n = 2p + n = 36
=> p = 12 ( p là số hiệu nguyên tử của Y)
Bạn tham khảo nha
Y2+ có : số hạt mang điện là [p + (e – 2)]
=> [p + (e – 2)] – n = 10
=> 2p – n = 12
Y2+ có 34 hạt cơ bản => Y có 34 + 2 = 36 hạt cơ bản
=> p + e + n = 2p + n = 36
=> p = 12 ( p là số hiệu nguyên tử của Y)

HD:
X- - 1e = X nên X có số hiệu điện tích Z = 10 - 1 = 9. X là Flo (F), KH: 919F

Ta có:
(2PM + NM) + 3(2PX + NX) = 196
(2PM + 3. 2PX) - (NM + 3NX) = 60
=> 2PM + 6PX = 128 và NM + 3NX = 68
Hay: PM + 3PX = 64. (1)
Mặt khác: (PM + NM ) - (PX + NX) = 8 và 2PM + NM + 1 - (2PX + NX - 3) = 16
=> (PM - PX) + (NM - NX) = 8 và (2PM - 2PX) + (NM - NX) = 12
=> PM - PX = 4 và NM - NX = 4. (2)
Từ (1) và (2) => PM = 19 và PX = 15
=> M là Kali và X là Photpho.
(Đề có dữ kiện bị sai tý X- nhiều hơn M3+ ta đã tự sửa rồi nhé ![]() )
)

Gọi Zm,Em,Nm là số proton,electron,notron của M.
Gọi Zx,Ex,Nx là số proton,electron,notron của X.
Theo đề bài ta có:
- Tổng số hạt proton,electron,notron là 196:
Zm+Em+Nm+3Zx+3Ex+3Nx=196(1)
- Số hạt mang điện nhiều hơn số hạt không mang điện là 60:
Zm+Em-Nm+3Zx+3Ex-3Nx=60(2)
- Tổng số 3 loại hạt trên trong ion M3+ ít hơn ion X- là 16:
-Zm-(Em-3)-Nm+Zx+Ex+1+Nx=16(3)
Từ (1),(2),(3) ta lập được hệ:
\(\left\{{}\begin{matrix}Zm+Em+Nm+3Zx+3Ex+3Nx=196\left(1\right)\\Zm+Em-Nm+3Zx+3Ex-3Nx=60\left(2\right)\\-Zm-\left(Em-3\right)-Nm+Zx+Ex+1+Nx=16\left(3\right)\end{matrix}\right.\)
Mà Z=E (=)
\(\left\{{}\begin{matrix}2Zm+Nm+6Zx+3Nx=196\left(1\right)\\2Zm-Nm+6Zx-3Nx=60\left(2\right)\\-2Zm-Nm+2Zx+Nx+3+1=16\left(3\right)\end{matrix}\right.\)
Lấy (1)+(2): 4Zm+12Zx=256(4)
Lấy (1)-(2): 2Nm+6Nx=136(5)
Từ (4) và (5) ta lập hệ pt:
\(\left\{{}\begin{matrix}\text{4Zm+12Zx=256(4)}\\2Nm+6Nx=136\left(5\right)\end{matrix}\right.\)
(=)\(\left\{{}\begin{matrix}Zm+3Zx=64\left(4\right)\\Nm+3Nx=68\left(5\right)\end{matrix}\right.\)
(=)\(\left\{{}\begin{matrix}Zm=64-3Zx\\Nm=68-3Nx\end{matrix}\right.\)
Thế Zm=64-3Zx và Nm=68-3Nx vào (3) có:
-2(64-3Zx)-(68-3Nx)+3+2Zx+Nx+1=16
(=) -128+6Zx-68+3Zx+3+2Zx+Nx+1=16
(=)8Zx+4Nx=208
(=)2Zx+Nx=52
(=)Nx=52-2Zx(*)
Áp dụng điều kiện của đồng vị bền:
\(1\le\dfrac{N}{Z}\le1.52\)
(=)\(\left\{{}\begin{matrix}Zx\le Nx\\1.52Zx\ge Nx\end{matrix}\right.\)
(=)\(\left\{{}\begin{matrix}Zx\le52-3Zx\\1.52Zx\ge52-3Zx\end{matrix}\right.\)
(=)\(\left\{{}\begin{matrix}Zx\le\dfrac{52}{3}\\Zx\ge\dfrac{52}{3.52}\end{matrix}\right.\)
(=)\(15\le Zx\le17\)
(=)Zx=\(\left\{{}\begin{matrix}15\\16\\17\end{matrix}\right.\)
Vì tìm X- nên chọn Zx=17.
Thế Zx=17 vào (*) có:
Nx=52-2(17)=18
=) X là Clo.
Clo: ô thứ 17,chu kì 3,nhóm VIIA.
Thế Zx=17 vào (4) có:
Zm+3(17)=64(=)Zm=13.
Thế Nx=18 vào (5) có:
Nm+3(18)=68(=)Nm=14.
=) M là Al.
Al: ô thứ 13,chu kì 3,nhóm IIIA.

Đáp án B
Gọi a, b là lần lượt tổng số proton và nơtron
Ta có: 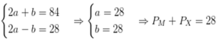
Ta có:
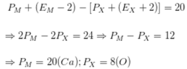
M là canxi ở ô 20, chu kì 4, nhóm IIA
Chọn B
