Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

p 1 V 1 = p 2 V 2 ⇒ p 1 = ( p 1 + 30.10 3 ) .16 24 = 60 K P a

a) Tính nhiệt độ ban đầu của khí.
Trong biến đổi đẳng áp, công của khí :
\(A'p\Delta V=\frac{m}{\mu}R\Delta T\Rightarrow\Delta T\frac{\mu\Delta'}{mR}=300K\)
Biến đổi đẳng áp : \(\frac{T_2}{T_1}=\frac{V_2}{V_1}=2\Rightarrow T_2=2T_1\)
\(\Delta T=T_2-T_1=T_1=300K\Rightarrow t_1=27^oC\)
b) Tính nhiệt lượng.
Biến đổi đẳng áp :\(Q=mc_p\Delta T=55200\left(J\right)\)
Tính \(\Delta U\)
c)Độ biến thiên nội năng của khí :
\(\Delta u=Q+A=Q-A'=39628\left(J\right)\)

Đáp án B
- Gọi p1 là áp suất của khí ứng vói V1 =9 (1)
- Gọi p2 là áp suất ứng với p2 = p1 + ∆p
Theo định luật luật Bôi-lơ-Ma-ri-ốt: p1V1 = p2 V2
9p1 = 6.(p1 + ∆p) ⟹ p1 - 2∆p = 2.40=80kPa

Áp dụng định luật Gay Luy-xac cho quá trình đẳng áp:
V1T1=V2T2V1T1=V2T2 suy ra T2=V2V1T1(1)T2=V2V1T1(1)
Áp dụng phương trình trạng thái cho trạng thái 1:
p1V1=mμRT1(2)p1V1=mμRT1(2)
Từ (1)(1) và (2)(2) rút ra: T2=μp1V2mRT2=μp1V2mR
Thay số μ=32g/mpl=32.10−3kg/molμ=32g/mpl=32.10−3kg/mol
p1=3atm=3.9,81.104N/m2;V2=11=10−3m3p1=3atm=3.9,81.104N/m2;V2=11=10−3m3, ta tìm được: T2=1133
Cho mình hỏi, tại sao bạn không đổi đơn vị của m=1 g ? Có cần phải đổi ra kg không?

Từ phương trình: \(p_V=nRT\)
Suy ra:
\(V=\frac{nRT}{p}=\frac{3\times8.31\times300}{600000}=0.012\left(m^3\right)=12\left(l\right)\)
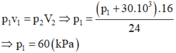
Đáp án B