Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Oxit cao nhất của một nguyên tố là RO3, theo bảng tuần hoàn suy ra công thức hợp chất khí với hiđro của nó là RH2, trong phân tử RH2, có 5,88% H về khối lượng
nên R có 100 - 5,88 = 94,12% về khối lượng
Trong phân tử RH2, có: 5,88% H là 2u
94,12% R là x u
Giải ra ta có x ≈ 32. Nguyên tử khối của R = 32. R là S. Công thức phân tử là SO3 và H2S.

6. Oxit cao nhất của 1 nguyên tố R ứng với công thức RO2. Nguyên tố R đó là
A. Magie. B. Nitơ. C. Cacbon. D. Photpho.
Chọn đáp án đúng.
C đúng.

F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
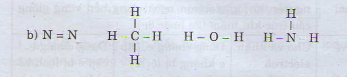
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.

Các bạn ơi giúp mình với. Chuyên đề này sáng mai mình phải nộp rồi! Cảm ơn các bạn nhiều!

RH4 -> RO2
%R= 53,3% => %O = 100-53,3= 46,7%
\(\dfrac{R}{53,3}\)=\(\dfrac{32}{46,7}\)
giải tìm R

Gọi hợp chất khí giữa R và H là: \(H_xR\)
Theo đề bài ta có:
\(\frac{1x}{M_R}=\frac{5,88}{94,12}\)
\(\Rightarrow M_R=\frac{94,12x}{5,88}=\frac{2353x}{147}\)
Lập bảng:
| x | 1 | 2 | 3 |
| MR | 16 (loại) | 32 (nhận) | 48(loại) |
\(\Rightarrow R:S\) (Lưu huỳnh)
Ta có: \(d_{Y/H_2}=\frac{M_Y}{M_{H_2}}\Rightarrow M_Y=32.2=64\)
\(CT:S_xO_y\)
\(\Rightarrow32x+16y=64\)
\(\Leftrightarrow2x+y=2\)
\(\Leftrightarrow2x=2-y\)
...............................
\(\Leftrightarrow\frac{x}{y}=\frac{1}{2}\)
\(\rightarrow CTHH:SO_2\)

3. Khối lượng mol của hợp chất đó là :
2.28 = 56 (g/mol)
mC = \(\frac{56.85,7}{100}\approx48\left(g\right)\)
mH = 56 - 48 = 8 (g)
nC = \(\frac{48}{12}=4\left(mol\right)\)
nH = \(\frac{8}{1}=8\left(mol\right)\)
Vậy công thức hóa học là C4H8.

a. 4Al + 3O\(_2\) -> 2Al2O3
4Fe + 3O2 -> 2Fe2O3
2Cu + O2 ->2CuO
Al2O3 + 3H2SO4 --->2Al2(SO4)3 + 3H2O
Fe2O3 + 3H2SO4 -->2Fe2(SO4)3 +3H2O
CuO + H2SO4 --> CuSO4 + H2O
b. no\(_2\) = (41,4 - 33,4) : 32 = 0,25 (mol)
Bảo toàn nguyên tố ta có
nH2SO4=2nO2=0,5(mol)
VH2SO4=0,5:1,14=0.44(ml)
VddH2SO4=0.44:20%=2.19(ml)

a) Có 3 lớp electron nên nằm ở chu kỳ 3 trong bảng HTTH. Lớp ngoài cùng có 3 electron nên cấu hình sẽ là 3s23p1. Như vậy cấu hình electron là 1s22s22p63s23p1 (Z= 13 là Al)
b) Có 2 lớp electron nên nằm ở chu kỳ 2 trong bảng HTTH. Lớp ngoài cùng có 2 electron nên cấu hình sẽ là 2s2. Như vật cấu hình electron là 1s22s2 (Z= 4 là Be)
c) đang đề cập tới là cấu hình electron của ion Fe3+ . Số hiệu nguyên tử của Fe là 26.
d) đang đề cập tới là cấu hình electron của ion Zn2+ .Số hiệu nguyên tử của Zn là 30

Một nguyên tố có 3electron hoá trị có công thức oxit cao nhất là
A. RO B. R2O3 C. RO2 D. R2O5