Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức hóa học của oxit là: S x O y
PTK của S x O y là: 32.x + 16.y (đvC)
Theo đề bài oxi chiếm 60% về khối lượng nên ta có:
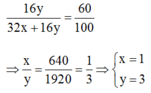
Vậy công thức hóa học của oxit là S O 3

Gọi công thức hóa học của oxit là: \(S_xO_y\)
\(PTK\) của \(S_xO_y\) là \(32x+16y\)
Theo đề bài oxi chiếm 60% về khối lượng nên ta có:
\(\dfrac{16y}{32x+16y}=\dfrac{60}{100}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{640}{1920}=\dfrac{1}{3}\Leftrightarrow\left[{}\begin{matrix}x=1\\y=3\end{matrix}\right.\)
Vậy CTHH của oxit là: \(SO_3\)

1.\(\dfrac{m_{Al}}{m_O}=\dfrac{9}{8}\)
\(Al_xO_y\)
\(x:y=\dfrac{9}{27}:\dfrac{8}{16}=\dfrac{1}{3}:\dfrac{1}{2}=2:3\)
Vậy CTHH là \(Al_2O_3\)
2.\(\rightarrow\%S=100-60=40\%\)
\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
Vậy CTHH là \(SO_3\)
3.
a.b.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=2.0,2=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,4 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
Chất dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,2\right).98=19,6g\)
c.Nồng độ gì bạn nhỉ?

Gọi CT dạng tổng quát của oxit lưu huỳnh cần tìm là SxOy (x,y: nguyên, dương).
Theo đề bài, ta có:
\(\frac{\%m_S}{32x}=\frac{\%m_O}{16y}\\ < =>\frac{40}{32x}=\frac{60}{16y}\\ < =>\frac{x}{y}=\frac{40.16}{32.60}=\frac{1}{3}\)
=> x=1; y=3
Với x=1; y=3 => CTPT của oxit lưu huỳnh cần tìm là SO3 (lưu huỳnh trioxit).
SO3 M Oxi = n phân tử Oxi *16
M Oxi/ M Oxi + 32= 0,6 => n phân tử oxi = 3

Phần trăm về khối lượng của nguyên tố lưu huỳnh trong oxit đó là:
\(\%m_S=100\%-\%m_O=100\%-60\%=40\%\)
Ta gọi công thức dạng chung của oxit cần tìm là SxOy (x,y: nguyên, dương)
Theo đề bài, ta có:
\(\frac{x}{y}=\frac{40}{32}:\frac{60}{16}=\frac{1}{3}\\ =>x=1;y=3\)
Vậy: CTHH của oxit cần tìm là SO3 (khi sunfurơ- hay còn gọi là lưu huỳnh trioxit)

Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)

\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
\(CTĐG:SO_3\)
\(CTCtrởthành:\left(SO_3\right)n=80\)
\(\Leftrightarrow n=1\)
Vậy CTHH: SO3
%mS=100-60=40%
Gọi công thức là SxOy
\(\dfrac{x}{y}=\)\(\dfrac{40}{32}:\dfrac{60}{16}\)=\(\dfrac{1}{3}\)
=>x=1 ,y=3
=>CTHH :SO3