Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- A tham gia phản ứng thế
=> A là : CH4
- B tham gia phản ứng cộng Br2 theo tỉ lệ 1 : 2
=> B là : C2H2
C là : C2H4
CTCT :

\(B:CH\equiv CH\)
\(C:CH_2=CH_2\)

\(n_{NaOH}=\dfrac{150.1,28.25\%}{40}=1,2\left(mol\right)\)
Dung dịch kiềm hấp thụ tối đa CO2 :
\(NaOH+CO_2\rightarrow NaHCO_3\)
=> \(n_{CO_2}=n_{NaOH}=1,2\left(mol\right)\)
=> \(V_{CO_2}=1,2.22,4=26,88\left(l\right)\)

Gọi công thức của ba hiđrocacbon đó là : C x H y , C a H b , C n H m
Khi đốt ta có :
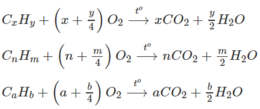
Vì số mol CO 2 tạo ra bằng 2 lần số mol hiđrocacbon đem đốt. Vậy theo phương trình hoá học của phản ứng cháy
→ X = a = n = 2.
Mặt khác : A không làm mất màu nước brom → không có liên kết đôi hoặc ba. Vậy A là CH 3 - CH 3
1 mol B chỉ tác dụng tối đa với 1 mol brom → có 1 liên kết đôi.
Vậy B là CH 2 = CH 2
1 mol C tác dụng tối đa với 2 mol brom → có liên kết ba.
Vậy C là CH ≡CH.

Chất có khả năng làm mất màu dung dịch Brom là Axetilen
C2H2+ Br2 ------> C2H2Br4

PTHH: \(CH_3-CH_2-C\equiv CH+2Br_2\rightarrow CH_3-CH_2-CBr_2-CHBr_2\)
0,2------------>0,4
=> \(m_{Br_2}=0,4.160=64\left(g\right)\)
PTHH:
\(CH_3-CH_2-C\equiv CH+2Br-Br\rightarrow CH_3-CH_2-CH_2-CHBr_2\)
0,2------------------------------->0,4
=> Mất màu tối đa 0,4 mol Br2

\(n_{CO_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(n_{H_2O}=\dfrac{5.4}{18}=0.3\left(mol\right)\)
\(a.\)
\(CT:C_xH_y\)
\(x:y=0.3:0.6=1:2\)
\(CT\text{nguyên }:\) \(\left(CH_2\right)_n\)
\(M_A=42\left(\text{g/mol}\right)\)
\(\Leftrightarrow14n=42\)
\(\Leftrightarrow n=3\)
\(CTPT:C_3H_6\)
\(b.\)
\(CH_2=CH-CH_3\)

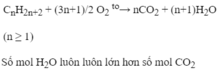
PTHH: C2H2 + 2Br2 -> C2H2Br4
=> Có khả năng kết hợp với 2 mol Br2