Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

+ Xét hh X : \(M_X=16\cdot3=48\)(g/mol)
Dùng phương pháp đường chéo:
SO2:64 O2:32 48 16 16 = 1 1
=> \(hhX\hept{\begin{cases}10\left(l\right)SO_2\\10\left(l\right)O_2\end{cases}}\)
=> \(hhY\hept{\begin{cases}8\left(l\right)SO_2\\10\left(l\right)O_2\end{cases}}\)=> \(M_Y=\frac{64\cdot8+32\cdot10}{18}=\frac{416}{9}\) (g/mol)
=> \(\frac{d_X}{d_Y}=\frac{M_X}{M_Y}=\frac{48}{\frac{416}{9}}=\frac{27}{26}\)
thank you, mình được thầy chữa r bn ms giải, tốt quá :((((

Giả sử các khí được đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
Gọi số mol CH4, C2H6 là a, b (mol)
=> \(a+b=\dfrac{25}{1}=25\left(mol\right)\) (1)
\(n_{O_2}=\dfrac{95}{1}=95\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a---->2a---------->a
2C2H6 + 7O2 --to--> 4CO2 + 6H2O
b------>3,5b-------->2b
=> \(\left\{{}\begin{matrix}n_{O_2\left(dư\right)}=95-2a-3,5b\left(mol\right)\\n_{CO_2}=a+2b\left(mol\right)\end{matrix}\right.\)
=> \(95-a-1,5b=\dfrac{60}{1}=60\)
=> a + 1,5b = 35 (2)
(1)(2) => a = 5; b = 20
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{5}{25}.100\%=20\%\\\%V_{C_2H_6}=\dfrac{20}{25}.100\%=80\%\end{matrix}\right.\)
\(\overline{M}_A=\dfrac{5.16+20.30}{5+20}=27,2\left(g/mol\right)\)
\(\overline{M}_B=20,5.2=41\left(g/mol\right)\)
=> \(d_{A/B}=\dfrac{27,2}{41}\approx0,663\)

\(n_{H_2}=\dfrac{12.10^{22}}{6.10^{23}}=0,2\left(mol\right)\); \(n_{N_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
=> mhh = 0,5.32 + 0,25.28 + 0,2.2 + 3,2 = 26,6(g)

PTHH: C3H8 +5O2 \(\underrightarrow{t^o}\) 3CO2 + 4H2O
2H2S + 3O2 \(\underrightarrow{t^o}\) 2SO2 + 2H2O
Gọi x và y lần lượt là số mol của C3H8 và H2S
-Theo PTHH ta có:
+nH2O = \(\dfrac{12,6}{18}=0,7\left(mol\right)\)
+nY=\(\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
⇒Hệ phương trình: \(\left\{{}\begin{matrix}4x+y=0,7\\3x+y=0,6\end{matrix}\right.\)
⇒x= 0,1 ; y= 0,3 (mol) (Cái này bấm máy tính giải hệ)
+nO2= 0,1.5 + 0,3.\(\dfrac{3}{2}\)=0,95(mol)
+VO2=0,95.22,5=21,28(lit)
- mX= 0,1.44 + 0,3.34 = 14,6(gam)
-MX=\(\dfrac{14,6}{0,4}=36,5\) g/mol
-\(\dfrac{\text{dX}}{H_2}\) = \(\dfrac{36,5}{2}=18,25\)

Bài 2:
a) Vì khối lượng mol của N2 và CO đều bằng 28 và lớn hơn khối lượng mol của khí metan CH4 (28>16)
=> \(d_{\dfrac{hhX}{CH_4}}=\dfrac{28}{16}=1,75\)
Hỗn hợp X nhẹ hơn không khí (28<29)
b)
\(M_{C_2H_4}=M_{N_2}=M_{CO}=28\left(\dfrac{g}{mol}\right)\\ \rightarrow M_{hhY}=28\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{Y}{H_2}}=\dfrac{28}{2}=14\)
c) \(\%V_{NO}=100\%-\left(30\%+30\%\right)=40\%\\ \rightarrow\%n_{CH_4}=40\%\\ Vì:\%m_{CH_4}=22,377\%\\ Nên:\dfrac{30\%.16}{40\%.30+30\%.16+30\%.\left(x.14+16\right)}=22,377\%\\ \Leftrightarrow x=-0,03\)
Sao lại âm ta, để xíu anh xem lại như nào nhé.
Bài 1:
\(a.\\ d_{\dfrac{SO_2}{O_2}}=\dfrac{64}{32}=2\\ d_{\dfrac{SO_2}{N_2}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{SO_3}}=\dfrac{64}{80}=0,8\\ d_{\dfrac{SO_2}{CO}}=\dfrac{64}{28}=\dfrac{16}{7}\\ d_{\dfrac{SO_2}{N_2O}}=\dfrac{64}{44}=\dfrac{16}{11}\\ d_{\dfrac{SO_2}{NO_2}}=\dfrac{64}{46}=\dfrac{32}{23}\\ b.M_{hhA}=\dfrac{1.64+1.32}{1+1}=48\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{hhA}{O_2}}=\dfrac{48}{32}=1,5\)

\(M_{hh}=\dfrac{M_{SO_2}.1+M_{O_2}.3}{1+3}=\dfrac{64.1+32.3}{4}=40\left(\dfrac{g}{mol}\right)\\ d_{\dfrac{hh}{O_2}}=\dfrac{40}{32}=1,25\)
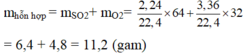
ta có M\(M_{honhop}=\frac{m_{honhop}}{n_{honhop}}=\frac{m_{o2}+m_{so2}}{0,1+0,05}=\frac{0,1\cdot32+0,05\cdot64}{0,15}\approx42,7\left(\frac{g}{mol}\right)\\ \)Vậy dhonhop/o2=\(\frac{M_{honhop}}{M_{o2}}=\frac{42,7}{32}\approx1,3\)(lần)