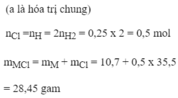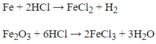Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

có n NO = 0,04 mol và dd có axit dư => ko tạo muối amoni
Al : x mol
Fe y mol
=> 27x + 56y = 1,95
3x +3y = 0,04.3
=> x =0,01 , y = 0,03
=> m Al = 0,27g, m Fe = 1,68 g
bạn gọi số mol của Fe(OH)2 : x mol
Fe(OH)3 : y mol
vì sau khi nung chỉ có Fe2O3 và Al2O3
0,015 0,0075
x + y = n Fe = 0,03 mol
n OH- = 4n Al 3+ - n kết tủa
=> 0,165 - 2x -3y = 4.0,03 - 0,015
=> 2x + 3y = 0,06
=> x = 0,03, y = 0 => Al đẩy Fe 3+ xuống Fe 2+ hoàn toàn
=> n Al tác dụng với HNO3 còn lại = 0,01 mol
=> n NO thoát ra = 0,01 mol
=> tổng n NO thoát ra = 0,05 mol
=> n HNO3 = 0,05.4 = 0,2 mol
=> Cm = 1,25 M

n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)

Gọi số mol Fe, Al là a,b
Khối lượng kim loại không tan là khối lượng của Cu
=> 56a + 27b = 9,08-2,4 = 6,68(g)
\(n_{H_2}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
______a------------------------>a
2Al + 6HCl --> 2AlCl3 + 3H2
_b------------------------->1,5b
=>a + 1,5b = 0,16 (mol)
=> a = 0,1; b = 0,04
=> mFe = 0,1.56 = 5,6 (g)
=> mAl = 0,04.27 = 1,08(g)

a) Bảo toàn nguyên tố H : \(n_{HCl}.1=2n_{H_2}=0,6\left(mol\right)\)
=> nH2=0,3(mol)
=> \(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b) Áp dụng định luật bảo toàn khối lượng :
\(m_{ct}=m_{kl}+m_{HCl}-m_{H_2}=10,4+0,6.36,5-0,3.2=31,7\left(g\right)\)

Gọi nAl=a mol
nMg=b mol
=>nH2=1,5a+b=1,68/22,4=0,075 mol
mhh cr=mAl+mMg=27a+24b=1,5
=>a=1/3 và b=0,025 mol
=>mAl=0,9gam
=>%mAl=0,9/1,5.100%=60% chọn A
Gọi số mol của Al và Mg lần lượt là x và y
pthh 2Al + 6HCl ---> 2AlCl3 + 3H2
x 1,5 x
Mg + 2HCl ---> MgCl2 + H2
y y
27x + 24y =1,5
ta có hệ phương trình
1,.5x + y =1,68/ 22,4
giải hệ phương trình ta được x= 1/30 , y= 0,025
----> m Al = 1/30 . 27= 0,9 (g)