Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


a)
CnH2n+2 + (1,5n + 0,5)O2 → nCO2 + (n + 1)H2O
1 → 1,5n + 0,5 n n + 1
Theo đề bài: nkhí trước pứ = nkhí sau pứ → 1 + 1,5n + 0,5 = n + n + 1 → n = 1
→ A: CH4
b)
R là chất dẻo nên R có thể là: PE, PVC, PA, PS → X có chứa liên kết đôi
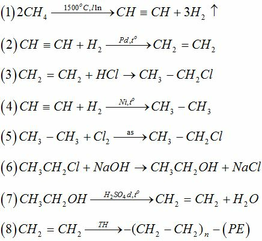

(a) Gọi CTPT của các chất là CxHyOz
M<170 => mC<170.55,8% => 12x<94,86 => x<7,9
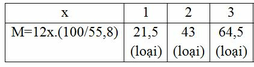
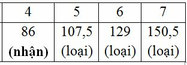
Vậy CTPT có dạng: C4HyOz (y≤10)(Do M là các số nguyên và là số chẵn)
Ta có: 12.4 + y + 16z = 86 => y + 16z = 38
+ z = 1: y = 22 (loại)
+ z = 2: y = 6 (nhận)
Vậy CTPT của các chất là: C4H6O2
b) A, B đều có nhóm CH3 và phản ứng với NaHCO3 tạo khí và chỉ có B có đồng phân hình học nên cấu tạo của A và B là:
A: CH2=C(CH3)-COOH
B: CH3-CH=CH-COOH
F, H, K có phản ứng với NaHCO3 tạo khí nên F, H, K là các axit.
- G là hợp chất không bền và chuyển hóa ngay thành G’ (G và G’ có cùng công thức phân tử) và khi oxy hóa bằng H2CrO4, hợp chất G’ chuyển hóa thành F nên G’ và F có cùng số nguyên tử C
C: CH3COOCH=CH2
F: CH3COOH
G: CH2=CH-OH
G’: CH3CHO
- H có phản ứng với NaHCO3 tạo khí nên H là axit. Mặt khác, phản ứng của H với bạc nitrat trong amoniac chỉ tạo thành các chất vô cơ nên H là HCOOH
D: HCOOCH2-CH=CH2
H: HCOOH
I: CH2=CH-CH2-OH
- L bị oxi hóa tạo HCOOH nên L là CH3OH
E: CH2=CH-COOCH3
K: CH2=CH-COOH
L: CH3OH
(1) CH2=C(CH3)-COOH (A) + NaHCO3 → CH2=C(CH3)-COONa + H2O + CO2
(2) CH3-CH=CH-COOH (B) + NaHCO3 → CH3-CH=CH-COONa + H2O + CO2
(3) CH3COOCH=CH2 (C) + NaOH → CH3COONa + CH3CHO (G’)
(4) CH3COONa + HCl → CH3COOH (F) + NaCl
(5) HCOOCH2-CH=CH2 (D) + NaOH → HCOONa + CH2=CH-CH2-OH (I)
(6) HCOONa + HCl → HCOOH (H) + NaCl
(7) CH2=CH-COOCH3 (E) + NaOH → CH2=CH-COONa + CH3OH (L)
(8) CH2=CH-COONa + HCl → CH2=CH-COOH (K) + NaCl
(9) CH3CHO + H2CrO4 → CH3COOH + H2CrO3
(10) CH3OH + 2H2CrO4 → HCOOH + 2H2CrO3 + H2O
(11) HCOOH + 2AgNO3 + 4NH3 + H2O → (NH4)2CO3 + 2Ag + 2NH4NO3
(c) Phản ứng polime hóa của A và C:
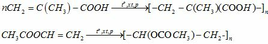
(d)


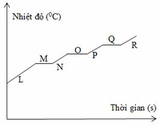
Ta thấy nhiệt độ sôi của oxi thấp nhất (-1830C) , sau đó đến argon (- 1860C ) và cuối cùng là nitơ (-1960C) => khi nâng dần nhiệt độ từ thấp nên cao ta sẽ thu được oxi trước => đến argon rồi đến nitơ
Nhiệt độ sôi của các chất là cố định, nên đoạn nằm ngang ( không biến thiên) chính là hằng số nhiệt độ sôi của các chất => đoạn MN là nhiệt độ sôi của oxi, đoạn OP là nhiệt độ sôi của Argon, đoạn OR là nhiệt độ sôi của nitơ.

Giá trị \(\Delta H\) và \(S\) của từng nguyên tử, phân tử bạn ghi rõ ra giúp mình.
Hướng dẫn:
a. Xét \(\Delta H\) của phản ứng = \(\Delta H\) sinh của sản phẩm - \(\Delta H\) sinh của chất tham gia
Với \(\Delta H\) > 0 thì phản ứng thu nhiệt và \(\Delta H\) < 0 thì phản ứng tỏa nhiệt
b. Xét \(\text{}\Delta G=\Delta H-T\Delta S\)
Với \(\Delta S=Scủasảnphẩm-Scủachấtthamgia\)
Với \(\Delta G\) < 0 thì pư tự diễn biến tại điều kiện T đang xét
Và ngược lại.
À mà đây đâu phải chương trình hóa lớp 9 đâu nhỉ??! Bạn tính học đội tuyển hóa cấp 3 hả?

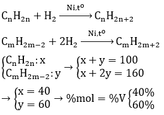
b, Vì phản ứng là tỏa nhiệt, nên để tăng hiệu suất cần giảm nhiệt độ. Tuy nhiên nếu hạ nhiệt độ quá thấp sẽ làm giảm tốc độ phản ứng, nên thực tế phản ứng này được tiến hành ở 850-900 độ C và có xúc tác Pt. Vì phản ứng thuận là chiều làm tăng số phân tử khí, nên để tăng hiệu suất phản ứng cần giảm áp suất. Tuy nhiên, điều kiện áp suất gây tăng giá thành công nghệ sản xuất, nên ta chỉ dùng áp suất thường (1 atm).
a, 4NH3 (k) + 5O2 (k) \(\rightarrow\) 4NO(k) + 6H2O(k)
\(\Delta\)H = 4\(\Delta\)HNO + 6\(\Delta\)H2O - 4\(\Delta\)HNH3
\(\Delta\)H = ( 4 . 90kJ ) + ( 6 . ( -242kJ ) ) - ( 4 . ( -46kJ ) = -908kJ