Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,Fe+2HCl\rightarrow FeCl_2+H_2\\ CuO+2HCl\rightarrow CuCl_2+H_2O\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\Rightarrow n_{Fe}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow\%m_{Fe}=\dfrac{0,1.56}{13,6}.100\%\approx41,176\%\\ \Rightarrow\%m_{CuO}\approx58,824\%\\ b,n_{CuO}=\dfrac{13,6-0,1.56}{80}=0,1\left(mol\right)\\ n_{HCl\left(p.ứ\right)}=2.\left(n_{Fe}+n_{CuO}\right)=2.\left(0,1+0,1\right)=0,4\left(mol\right)\\ \Rightarrow V_{ddHCl}=\dfrac{0,4}{2}=0,2\left(l\right)\)

Gọi số mol của Fe2O3 là x.
Gọi số mol của CuO là y.
Ta có PTHH:
Fe2O3 + 3H2 -> 2Fe + 3H2O
x 3x 2x 3x (mol)
CuO + H2 -> H2O + Cu
y y y y (mol)
Ta có
mchất rắn = 30,4 (g)
=> 64y + 56.2x = 30,4 (g)
=> 64y + 112x = 30,4 (g) (1)
Ta có:
mhỗn hợp = 32 (g)
=> 160x + 80y = 32(g) (2)
Từ (1) và (2), suy ra:
x=0,09
y=0,22
Ta có:
nH2(1) = 0,09. 3 = 0,27(mol)
=> VH2 = 0,27. 22,4 = 6,048(l)
Ta có:
nH2= 0,22 (mol)
=> VH2 = 0,22. 22,4 = 4,928 (l)
=> VH2 = 6,048 + 4,928 = 10,976(l)
Bạn kiểm tra lại đề bài đi xem có đúng không chứ mình thấy nó cứ sao sao ý. Tính toàn ra số âm không à.

- Từ giả thiết tính được : n Cl 2 = 0,035 mol; n O 2 = 0,025 mol
Theo ĐLBT khối lượng :
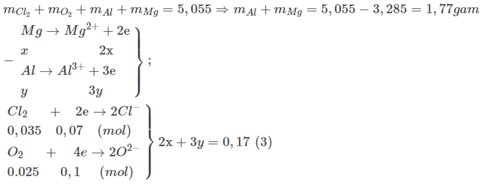
Từ (3)(4) ⇒ x = 0,04; y = 0,03
⇒ m Mg = 0,04.24 = 0,96g; m Al = 0,03.27 = 0,81g
Phản ứng không oxi hoá - khử

Fe không tác dụng với H2SO4 đặc nguội
=> mFe = 5,6 (g)
Gọi số mol Mg, Cu là a, b (mol)
=> 24a + 64b = 14,4 - 5,6 = 8,8 (1)
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Mg + 2H2SO4 --> MgSO4 + SO2 + H2O
a---------------------------->a
Cu + H2SO4 --> CuSO4 + SO2 + H2O
b--------------------------->b
=> a + b = 0,2 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{14,4}.100\%=38,89\%\\\%m_{Mg}=\dfrac{0,1.24}{14,4}.100\%=16,67\%\\\%m_{Cu}=\dfrac{0,1.64}{14,4}.100\%=44,44\%\end{matrix}\right.\)

Gọi \(\left\{{}\begin{matrix}n_{CuO}=x\\n_{MgO}=y\end{matrix}\right.\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x x ( mol )
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}80x+40y=16\\135x+95y=32,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{CuO}=0,1.80=8g\)
\(\Rightarrow m_{MgO}=0,2.40=8g\)
\(\%m_{CuO}=\dfrac{8}{16}.100=50\%\)
\(\%m_{MgO}=\dfrac{8}{16}.100=50\%\)
\(m_{CuCl_2}=0,1.135=13,5g\)
\(m_{MgCl_2}=0,2.95=19g\)

a, Ta có: $n_{O}=0,6(mol)$
Suy ra $n_{H^+/pu}=1,2(mol)\Rightarrow n_{H_2SO_4}=0,6(mol)$
Bảo toàn khối lượng ta có: $m_{muoi}=29,6+0,6.96=87,2(g)$

mg+2hcl-> mgcl2+h2
0,05 0,1 0,05 <-1,12/22,4
mgo+2hcl-> mgcl2+h2o
0,19->0,38 0,19
mmgo=8,8-0,05*24=7,6-> nmgo=7,6/40=0,19
%mmgo=7,6/8,8*100=86,36%
%mmg=100-8636=13,63%
mhcl=(0,38+0,1)*36,5=17,52
mddhcl=17,52*100/14,6=120
mddsau pư= 120+8,8-0,05*2=128,7
C%mgcl2= (0,05+0,19)*95/128,7*100=17,71%


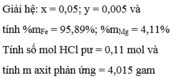
mO trong CuO=16,8-14,4=2,4(g)
nO trong CuO=0,15(mol)
Ta có:
nCuO=nO=0,15(mol)
mCuO=0,15.80=12(g)
mmgO=16,8-12=4,8(g)