
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 1:
Ta có : 1 mol muối RCO3 (có khối lượng = R + 60n) chuyển thành 1 mol RCln (có khối lượng = R + 71n)
=> khối lượng tăng = 71n – 60n = 11n gam
=> Khi chuyển 1 mol gốc CO3 thành 2 mol gốc Cl và tạo ra 1 mol CO2 thì khối lượng tăng 11 gam
a) Ta có công thức tính nhanh sau : \(m_{muốiclorua}=n_{muốicacbonat}+11.n_{CO_2}\)
=> \(n_{CO_2}=\dfrac{11,1-10}{11}=0,1\left(mol\right)\)
=> \(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
b) \(MCO_3+2HCl\rightarrow MCl_2+CO_2+H_2O\)
\(n_{HCl}=2n_{CO_2}=0,2\left(mol\right)\)
=> \(m_{ddHCl}=\dfrac{0,2.36,5}{3,65\%}=200\left(g\right)\)
c) \(m_{ddsaupu}=10+200-0,1.44=205,6\left(g\right)\)
\(C\%_{muối}=\dfrac{11,1}{205,6}.100=5,4\%\)
d) \(n_{MCO_3}=n_{MCl_2}\)
=> \(\dfrac{10}{M+60}=\dfrac{11,1}{M+71}\)
=> \(M=40\left(Ca\right)\)

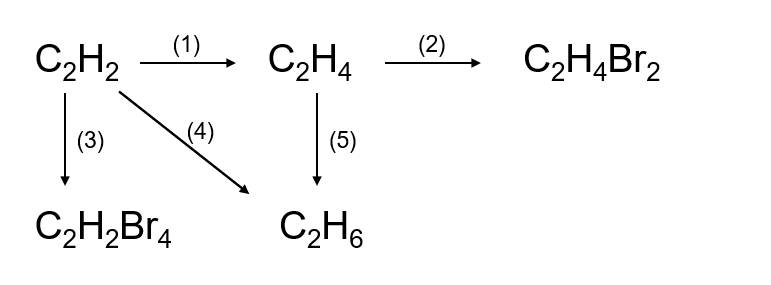
(1) \(2CH_4\xrightarrow[lln]{1500^oC}C_2H_2+3H_2\)
(2) \(C_2H_2+H_2\underrightarrow{t^o,Pd}C_2H_4\)
(3) \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
(4) \(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
(5) \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
(6) \(C_2H_2+2H_2\underrightarrow{t^o,Ni}C_2H_6\)
(7) \(C_2H_4+H_2\underrightarrow{t^o,Ni}C_2H_6\)
(1) 2��4→���1500���2�2+3�22CH41500oCllnC2H2+3H2
(2) �2�2+�2��,��→�2�4C2H2+H2to,PdC2H4
(3) �2�4+��2→�2�4��2C2H4+Br2→C2H4Br2
(4) ��4+��2��→��3��+���CH

alo giúp mik Nhân dịp đi du lịch về, Mai mang đến lớp 51 móc chìa khóa để tặng cho cácbạn. Sau khi chia hết cho các bạn (tính cả mình) thì Mai còn thừa3chiếc. Hỏi lớpMai có bao nhiêu bạn, biết số học sinh nhiều hơn 20 và ít hơn 30 bạn.

Bài 2) Ở 90 độ C:
- 100 gam nước hoà tan 50 gam KCl để tạo 150 gam dung dịch bão hoà ở nhiệt độ này
a) C% của dung dịch bão hoà tại 90 độ C là:
(Khối lượng chất tan/Khối lượng dung dịch) . 100%
<=> (50:150).100% = 33,33%
b) Ở 0 độ C:
Gọi m là khối lượng chất tan KCl ở 0o C => Khối lượng dung dịch tại nhiệt độ này là: 100+m
Theo đề bài ra ta có: m/100+m = 25,93%
=> m = 35 gam
Vậy ở 0 độ C độ tan của KCl trong nước là 35 gam
c) Ở 90 độ C:
100 gam nước hoà tan 50 gam KCl tạo 150 gam dd
=> 600 gam dung dịch tạo 200 gam KCl và 400 gam nước
- Ở 0 độ C:
100 gam nước hoà tan 35 gam KCl tạo 135 gam dd
=> 400 gam nước hoà tan được 140 gam KCl tạo 400 + 140 = 540 gam dung dịch
Vậy khi làm lạnh 600 gam dung dịch KCl từ 90 độ xuống 0 độ thì khối lượng dung dịch thu được là 540 gam

Đề bài cho hỗn hợp X gồm hai khí là methane (CH4) và ethylene (C2H4). Hỗn hợp này có tỉ khối so với hydrogen (H2) bằng 10.
- Bước 1: Tính khối lượng mol trung bình của hỗn hợp X (MX)
Tỉ khối của hỗn hợp X so với hydrogen được tính bằng công thức: dX/H2=MH2MX.
Trong đó, MH2=2 g/mol.
Ta có: 10=2MX⇒MX=10×2=20 g/mol.
- Bước 2: Gọi thành phần phần trăm thể tích của từng khí trong hỗn hợp
Giả sử trong 1 mol hỗn hợp X, số mol của CH4 là x và số mol của C2H4 là y.
Ta có: x+y=1 (1)
Khối lượng mol trung bình của hỗn hợp X được tính bằng công thức: MX=nCH4+nC2H4nCH4⋅MCH4+nC2H4⋅MC2H4.
MCH4=12+4=16 g/mol.
MC2H4=12×2+4=28 g/mol.
Thay vào công thức ta có: 20=x+yx⋅16+y⋅28=116x+28y (2)
Từ (1) và (2) ta có hệ phương trình:
x+y=1
16x+28y=20
Giải hệ phương trình này, ta được: x=32 và y=31.
Điều này có nghĩa là trong hỗn hợp X, số mol của CH4 chiếm 32 và số mol của C2H4 chiếm 31.
- Bước 3: Tính tổng số mol của hỗn hợp X
Thể tích của hỗn hợp X ở điều kiện tiêu chuẩn (đktc) là 3,7185 lít.
Số mol của hỗn hợp X là: nX=24.79V=24.793.7185=0.15 mol.
(Lưu ý: Nếu đề bài cho ở điều kiện tiêu chuẩn cũ (0 độ C, 1 atm) thì V = 22.4, nhưng theo quy ước quốc tế mới, 1 bar và 25 độ C thì V = 24.79. Đề bài không nói rõ nên ta chọn chuẩn mới là 24.79).
- Bước 4: Tính số mol C2H4 trong hỗn hợp X
Từ kết quả ở bước 2, ta biết số mol C2H4 chiếm 31 tổng số mol.
nC2H4=nX×y=0.15×31=0.05 mol.
- Bước 5: Tính số mol Br2 đã phản ứng
Khi hỗn hợp X cho qua dung dịch Br2 dư, chỉ có ethylene (C2H4) phản ứng vì nó có liên kết đôi (C=C). Methane (CH4) là ankan nên không phản ứng với Br2.
Phương trình phản ứng:
C2H4+Br2→C2H4Br2
Theo phương trình, tỉ lệ mol là 1:1, vậy:
nBr2=nC2H4=0.05 mol.
Kết luận
Số mol Br2 đã tham gia phản ứng là 0,05 mol.

Bạn chỉ cần nhớ dãy hoạt động hóa học: K, Na, Ca, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Hg, Ag, Pt, Au để biết phản ứng giữa muối và kim loại có xảy ra hay không vì chỉ có kim loại mạnh hơn trong dãy mới có thể đẩy được kim loại yếu hơn ra khỏi muối của nó để tạo thành muối mới và kim loại mới.
VD: Các phản ứng sau là không xảy ra:
\(Al\left(NO_3\right)_3+Cu\) vì Cu đứng sau Al trong dãy.

1) 3Fe+2O2\(\overset{t^0}{\rightarrow}\)Fe3O4
2) Fe3O4+4H2SO4\(\rightarrow\)FeSO4+Fe2(SO4)3+4H2O
3) Fe+2HCl\(\rightarrow\)FeCl2+H2
4) FeCl2+2NaOH\(\rightarrow\)Fe(OH)2+2NaCl
5) Fe(OH)2+H2SO4\(\rightarrow\)FeSO4+2H2O
6) 2Fe+3Cl2\(\rightarrow\)2FeCl3
7) FeCl3+3NaOH\(\rightarrow\)Fe(OH)3+3NaCl
8) 2Fe(OH)3\(\overset{t^0}{\rightarrow}\)Fe2O3+3H2O
9) Fe2O3+3H2SO4\(\rightarrow\)Fe2(SO4)3+3H2O
10) Fe2(SO4)3+3NaOH\(\rightarrow\)2Fe(OH)3+3Na2SO4







- Hợp chất vô cơ: CO2, Na2CO3
- Hợp chất hữu cơ:
+ Hiđrocacbon: C4H10, C6H6, C3H4
+ Dẫn xuất của hiđrocacbon: C3H8O, CH3Cl, C6H6Cl6