
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


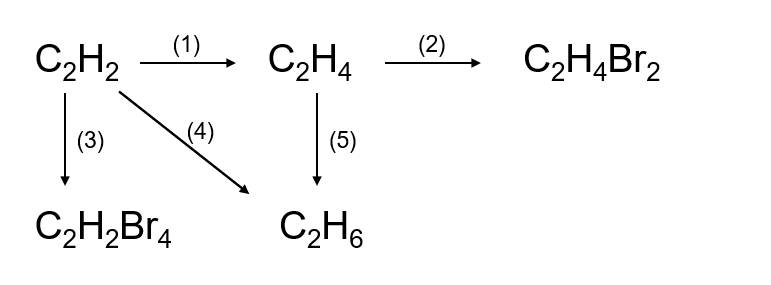
(1) \(2CH_4\xrightarrow[lln]{1500^oC}C_2H_2+3H_2\)
(2) \(C_2H_2+H_2\underrightarrow{t^o,Pd}C_2H_4\)
(3) \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
(4) \(CH_4+Cl_2\underrightarrow{as}CH_3Cl+HCl\)
(5) \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
(6) \(C_2H_2+2H_2\underrightarrow{t^o,Ni}C_2H_6\)
(7) \(C_2H_4+H_2\underrightarrow{t^o,Ni}C_2H_6\)
(1) 2��4→���1500���2�2+3�22CH41500oCllnC2H2+3H2
(2) �2�2+�2��,��→�2�4C2H2+H2to,PdC2H4
(3) �2�4+��2→�2�4��2C2H4+Br2→C2H4Br2
(4) ��4+��2��→��3��+���CH4+Cl2asCH3Cl+HCl
(5) �2�2+2��2→�2�2��4C2H2+2Br2→C2H2Br4
(6) �2�2+2�2��,��→�2�6C2H2+2H2to,NiC2H6
(7) �2�4+�2��,��→�2�6C2H4+H2to,NiC2H6

12.
Na2CO3+H2SO4->Na2SO4+H2O+CO2
............. 0,5 ............. ......... 0,5
CO2+2KOH->K2CO3+H2O
x 2x x
CO2+KOH->KHCO3
y y y
mKOH=98.40/100=39,2g
nKOH=39,2/56=0,7mol
Có:
2x+y=0,7
138x+100y=57,6
=>x=0,2mol; y=0,3mol
mK2CO3=138.0,2=27,6g
mKHCO3=57,6-27,6=30g
b.
nCO2=x+y=0,2+0,3=0,5mol
CMddH2SO4=0,5/0,2=2,5M
8. Hoàn thành sơ đồ chuyển hóa sau:
Mg \(\underrightarrow{\left(1\right)}\) MgO \(\underrightarrow{\left(2\right)}\) MgCl2 \(\underrightarrow{\left(3\right)}\) Mg(OH)2 \(\underrightarrow{\left(4\right)}\) MgO \(\underrightarrow{\left(5\right)}\) MgSO4 \(\underrightarrow{\left(6\right)}\) MgCO3 \(\underrightarrow{\left(7\right)}\) MgO
\(\left(1\right)2Mg+O_2\underrightarrow{t^o}2MgO\)
\(\left(2\right)MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(\left(3\right)MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
\(\left(4\right)Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
\(\left(5\right)MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(\left(6\right)MgSO_4+Na_2CO_3\rightarrow MgCO_3+Na_2SO_4\)
\(\left(7\right)MgCO_3\underrightarrow{t^o}MgO+CO_2\uparrow\)




1) 3Fe+2O2\(\overset{t^0}{\rightarrow}\)Fe3O4
2) Fe3O4+4H2SO4\(\rightarrow\)FeSO4+Fe2(SO4)3+4H2O
3) Fe+2HCl\(\rightarrow\)FeCl2+H2
4) FeCl2+2NaOH\(\rightarrow\)Fe(OH)2+2NaCl
5) Fe(OH)2+H2SO4\(\rightarrow\)FeSO4+2H2O
6) 2Fe+3Cl2\(\rightarrow\)2FeCl3
7) FeCl3+3NaOH\(\rightarrow\)Fe(OH)3+3NaCl
8) 2Fe(OH)3\(\overset{t^0}{\rightarrow}\)Fe2O3+3H2O
9) Fe2O3+3H2SO4\(\rightarrow\)Fe2(SO4)3+3H2O
10) Fe2(SO4)3+3NaOH\(\rightarrow\)2Fe(OH)3+3Na2SO4

Cách 1:
Cho vào dd HCl ta thu dc đồng ko tan
2Al + 6HCl -> 2AlCl3 + 3H2
Cách 2:
Cho vào dd kiềm dư như NaOH thu được đồng ko tan
2Al + 2NaOH + 2H2O -> 2NaAlO2 + 3H2

PTHH : Al + HCl => AlCl3 + H2
Fe + HCl => FeCl2 + H2
a. nHCl = CM. V = 1.0,7 = 0,7 (mol)
Đặt số mol của Al =x ; Fe =y
PTHH : 2Al +6HCl => 2AlCl3 + 3H2
x -> 3x
Fe + 2HCl => FeCl2 + H2
y -> 2y
Ta có : x.27 + y.56 = 43,9 (g)
3x +2y = 0,7 (mol)
( cậu dùng máy tính giải hệ pt 2 ẩn nhé, tớ hiện không có máy tính )
=> x=...
y=....
Từ x,y suy ra số mol trên 2 pt của H2 rồi cộng lại với nhau => V=n.22,4
b. tính mFe, mAl
%mFe= \(\dfrac{mFe}{43,9}\).100% =
%mAl = \(\dfrac{mAl}{43,9}\).100% =
c.Vdd pư = Vdd bđ =0,7 (l)
CM AlCl3 =\(\dfrac{nAlCl_3}{Vddpư}\)=
CM FeCl2 = \(\dfrac{nFeCl_2}{Vddpu}\)=
Lần sau em nhớ xoay ảnh về đúng chiều để cô và các bạn dễ quan sát câu hỏi nhé

A là dung dịch H2SO4
B: Na2CO3
C: H2SO4 đặc
D: Xút (NaOH)
Khi cho DD H2SO4 tác dụng với Na2CO3 giải phóng khí SO2 mang theo hơi nước.
Bình C để giữ hơi nước lại trong bình (H2SO4 đặc háu nước) SO2 không tác dụng tiếp tục được dẫn qua bình đựng.
Để tránh SO2 thoát ra bên ngoài gây ô nhiễm môi trường và 1 số bệnh cho con người nên Xút được đặt ở miệng bình để tạo muối.

a;Zn + 2HCl\(\rightarrow\)ZnCl2+H2
Zn+ H2SO4\(\rightarrow\)ZnSO4+H2
b;TN1:
\(\sum n_{H_2}=0,1+0,1=0,2\left(mol\right)\)
VH2=22,4.0,2=4,48(lít)
TN2:
\(\sum n_{H_2}=0,1+0,05=0,15\left(mol\right)\)
VH2=22,4.0,15=3,36(lít)
Vậy ở TN1 sinh ra nhiều H2 hơn




 mn giúp e những câu còn lại ạ :)
mn giúp e những câu còn lại ạ :)

 giup mình với. Mình cần rất gấp
giup mình với. Mình cần rất gấp

 Bài 5.5 ạ
Bài 5.5 ạ
\(n_{Cu\left(NO_3\right)_2}=0,2.2=0,4\left(mol\right)\)
Gọi x là số mol của thanh nhôm phản ứng với dung dịch \(Cu\left(NO_3\right)_2\)
PTHH:
\(2Al+3Cu\left(NO_3\right)_2\rightarrow2Al\left(NO_3\right)_3+3Cu\)
x---------------------------------------->1,5x
Theo đl tăng giảm khối lượng có:
\(m_{Cu}-m_{Al}=64.1,5x-27x=43,8-30=13,8\)
=> \(x=0,2\)
\(n_{Cu\left(NO_3\right)_2.dư}=0,4-1,5.0,2=0,1\left(mol\right)\)
\(n_{Al\left(NO_3\right)_3}=x=0,2\left(mol\right)\)
\(CM_{Cu\left(NO_3\right)_2}=\dfrac{0,1}{0,2}=0,5M\\ CM_{Al\left(NO_3\right)_3}=\dfrac{0,2}{0,2}=1M\)