Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1)
a) 2HgO\(-t^0\rightarrow2Hg+O_2\)
b)Theo gt: \(n_{HgO}=\frac{2,17}{96}\approx0,023\left(mol\right)\\ \)
theo PTHH : \(n_{O2}=\frac{1}{2}n_{HgO}=\frac{1}{2}\cdot0,023=0,0115\left(mol\right)\\ \Rightarrow m_{O2}=0,0115\cdot32=0,368\left(g\right)\)
c)theo gt:\(n_{HgO}=0,5\left(mol\right)\)
theo PTHH : \(n_{Hg}=n_{HgO}=0,5\left(mol\right)\\ \Rightarrow m_{Hg}=0,5\cdot80=40\left(g\right)\)
Câu 2)
a)PTHH : \(S+O_2-t^0\rightarrow SO_2\)
b)theo gt: \(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
theo PTHH \(n_S=n_{SO2}=0,1\left(mol\right)\\ \Rightarrow m_S=0,1\cdot32=3,2\left(g\right)\)
Ta có khối lượng S tham gia là 3,25 g , khối lượng S phản ứng là 3,2 g
Độ tinh khiết của mẫu lưu huỳnh là \(\frac{3,2}{3,25}\cdot100\%\approx98,4\%\)
c)the PTHH \(n_{O2}=n_{SO2}=0,1\left(mol\right)\Rightarrow m_{O2}=0,1\cdot32=3,2\left(g\right)\)

a/ Ta có: K : hóa trị 1
Cl : hóa trị 1
=> x =1 ; y = 1
=> CT: KCl
b/ 2KClO3 ==( nhiệt)==> 2KCl + 3O2
c/ Áp dụng định luật bảo toàn khối lượng
=> mO2 = mKClO3 - mKCl = 4,5 - 14,9 = -10,4
Chỗ này hình như bạn sai đề bài rồi nhé!!!!
Bạn xem lại đề bài thấy số liệu khác thì cứ theo cách này mà làm nhé!!!

a. Chất dùng để điều chế O2 trong phòng thí nghiệm là KClO3
PTHH : 2KClO3 -> 2KCl + 3O2 <ở to>
b. Chất dùng để điều chế H2 trong phòng thí nghiệm là :HCl, Zn <Ko bt câu này đúng ko>
PTHH: Zn + 2HCl -> ZnCl2 + H2
c. Hai chất tác dụng với nhau tạo ra Ca<OH>2 là : CaO và H2O
PTHH: CaO + H2O -> Ca<OH>2
d. Hai chất tác dụng với nhau tạo ra H3PO4 là : P2O5 và H2O
PTHH: P2O5 + 3H2O -> 2H3PO4
Mình thay dấu ngoặc đơn thành dấu ngoặc kép, vì mình ko ghi đc. Bn thông cảm nha.

a, Cac chat co the dieu che hidro la
Zn , Al , Cu , H2O tac dung voi dd HCl va H2SO4
Phuong trinh hoa hoc
Zn + HCl \(\rightarrow\) ZnCl2 + H2
Zn + H2SO4 \(\rightarrow\) ZnSO4 + H2
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2
Cu + H2SO4 \(\rightarrow\) CuSO4 + H2
Cu + 2HCl \(\rightarrow\) CuCl2 + H2
2H2O\(\underrightarrow{dienphan}\) 2H2 + O2
b, Cac chat co the dung de dieu che O2 la
H2O , KMnO4 , KClO3
KMnO4 \(\underrightarrow{t0}\) K2MnO4 + MnO2 + O2
KClO3 \(\underrightarrow{to}KCl+O2\)
H2O \(\underrightarrow{dienphan}\) H2 + O2
Ở ý a e sai ở pt điều chế H2 từ Cu: Cu không tác dụng với H2SO4 loãng và HCl

Ta có : PT1 : 2KClO3 ----> 2KCl + 3O2
PT2 : 2KMnO4 ----> K2MnO4 + MnO2 + O2
Gọi khối lượng của KClO3 và KMnO4 là x
*PT1 : \(n_{KClO_3}=\frac{x}{M}=\frac{x}{122,5}\)
\(n_{O_2}=\frac{3}{2}n_{KClO_3}=\frac{3}{2}.\frac{x}{122,5}=\frac{3x}{245}\)
*PT2 \(n_{KMnO_4}=\frac{x}{M}=\frac{x}{158}\)
Nhận thấy \(\frac{3x}{245}>\frac{x}{158}\)=> Dùng KClO3 cho nhiều O2 hơn

Câu 1/ oxi nặng hơn hidro vì
A. Khối lượng mol oxi lớn hơn khối lượng mol hidro
B. Oxi là đơn chất
C. Không khí là 1 hỗn hợp
Câu 2/ oxi là
A. Đơn chất. B. hợp chất C. nguyên tử
Câu 3/ phản ứng thể hiện sự oxi hóa là :
A.Ba + O2 -> BaO
- Sự oxi hóa là sự tác dụng của oxi với 1 chất
B. Na + H2O -> NaOH + H2
C.K2O + H2O -> KOH
Câu 4/ oxi được điều chế từ
A. KMnO4. B. CaCO3 C.NaOH
- PTHH: \(2KMnO_4-t^o>K_2MnO_4+MnO_2+O_2\uparrow\)
Câu 5 / được 1,2 gam Cacbon trong khí oxi thu được cacbon dioxit
a. Viết phương trình phản ứng
b. Tính thể tích khí oxi tham gia ( đktc)
c. Tính thể tích khí cacbon điôxit tạo thành(đktc)d.d
d. Nếu cho 1,2 gam các bon tác dụng với 2,24 lít Oxi (đktc) thì chất nào dư?
Giải:
\(n_C=\dfrac{1,2}{12}=0,1\left(mol\right)\)
- a. PTHH: \(C+O_2-t^o->CO_2\uparrow\)
b. Theo PT ta có: \(n_{O_2}=n_C=0,1\left(mol\right)\)
=> \(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
c, Theo PT ta có: \(n_{CO_2}=n_C=0,1\left(mol\right)\)
=> \(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
d. \(n_C=\dfrac{1,2}{12}=0,1\left(mol\right)\)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Lập tỉ lệ: \(\dfrac{0,1}{1}=\dfrac{0,1}{1}\Rightarrow\) C và O2 đều pư hết, không chất nào dư.

Giả sử ta lấy cùng một khối lượng là a g
Vậy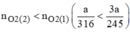 nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3
nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3