Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 2. \(n_{Cl_2}=\frac{11,2}{22,4}=0,5\left(mol\right)\);\(n_{NaI}=\frac{60}{150}=0,4\left(mol\right)\)
PTHH: \(Cl_2+2NaI\rightarrow2NaCl+I_2\uparrow\)
TheoPT:1..........2.........(mol)
Theo ĐB:0,5......0,4
Lập tỉ lệ: \(\frac{0,5}{1}>\frac{0,4}{2}\)=> Cl2 dư, NaI phản ứng hết
Theo phương trình : \(n_{I_2}=\frac{1}{2}n_{NaI}=0,2\left(mol\right)\)
\(n_{Cl_2\left(pứ\right)}=\frac{1}{2}n_{NaI}=0,2\left(mol\right)\)
\(n_{Cl_2\left(dư\right)}=0,5-0,2=0,3\left(mol\right)\)
Cl2 dư phản ứng với I2 vừa sinh ra
PTHH: \(5Cl_2+I_2+6H_2O\rightarrow10HCl+3HIO_3\)
Lập tỉ lệ giữa Cl2 và I2: \(\frac{0,3}{5}< \frac{0,2}{1}\)=> I2 dư
Theo PT : \(n_{I_2\left(pứ\right)}=0,06\left(mol\right)\)
\(\Rightarrow n_{I_2\left(dư\right)}=0,2-0,06=0,14\left(mol\right)\)
Vậy khối lượng I2 sau phản ứng: \(m_{I_2\left(dư\right)}=0,14.127.2=35,56\left(g\right)\)

a) \(n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,05<-----------0,05---->0,075
=> \(\%Al=\dfrac{0,05.27}{14,15}.100\%=9,54\%\)
=> \(\%Cu=\dfrac{14,15-0,05.27}{14,15}.100\%=90,46\%\)
b) \(V_{H_2}=0,075.22,4=1,68\left(l\right)\)
c) \(n_{Cu}=\dfrac{14,15-0,05.27}{64}=0,2\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
2Cu + O2 --to--> 2CuO
0,2-->0,1
=> \(V_{O_2}=\left(0,1+0,0375\right).22,4=3,08\left(l\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ m_{AlCl_3}=6,675\left(mol\right)\\ n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\\ \Rightarrow n_{Al}=n_{AlCl_3}=0,05\left(mol\right)\\ \Rightarrow m_A=0,05.27=1,35\left(g\right);m_{Cu}=14,15-1,35=12,8\left(g\right)\\ \%m_{Cu}=\dfrac{12,8}{14,15}.100\approx90,459\%\\ \Rightarrow\%m_{Al}\approx9,541\%\\ b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\\ n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,05=0,075\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,075.22,4=1,68\left(l\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{O_2}=\dfrac{3}{4}.n_{Al}+\dfrac{1}{2}.n_{Cu}=\dfrac{3}{4}.0,05+\dfrac{1}{2}.0,2=0,0875\left(mol\right)\)
\(\Rightarrow V_{O_2\left(đktc\right)}=0,0875.22,4=1,96\left(l\right)\)

Đáp án B
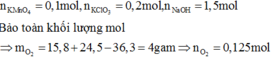
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()
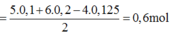


Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.





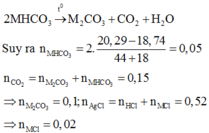
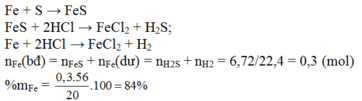
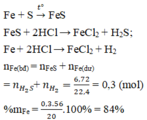
Bài này có dư thiếu gì khong bro ;<<
Không dư mà cũng chẳng thiếu