Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
- Trong A chứa Al, Cu, Ag
- Do trong A chứa Cu => Ag bị đẩy ra hết khỏi dd
- Do cho B tác dụng với NaOH dư thu được kết tủa
=> Trong B chứa Al(NO3)3, Cu(NO3)2
Al + 3AgNO3 --> Al(NO3)3 + 3Ag
2Al + 3Cu(NO3)2 --> 2Al(NO3)3 + 3Cu
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
Al(NO3)3 + 3NaOH --> Al(OH)3 + 3NaNO3
Al(OH)3 + NaOH --> NaAlO2 + 2H2O
Cu(NO3)2 + 2NaOH --> Cu(OH)2 + 2NaNO3
Cu(OH)2 --to--> CuO + H2O
2)
Rắn sau khi nung là CuO
\(n_{CuO}=\dfrac{1,6}{80}=0,02\left(mol\right)\)
=> \(n_{Cu\left(NO_3\right)_2\left(B\right)}=0,02\left(mol\right)\)
\(n_{H_2}=\dfrac{0,1008}{22,4}=0,0045\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,003<---------------------------------0,0045
Bảo toàn Al: \(n_{Al\left(NO_3\right)_3\left(B\right)}=\dfrac{0,81}{27}-0,003=0,027\left(mol\right)\)
Gọi số mol Cu, Ag trong hỗn hợp kim loại là a, b (mol)
=> 64a + 108b = 6,012 (1)
Bảo toàn Ag: \(n_{AgNO_3\left(X\right)}=b\left(mol\right)\)
Bảo toàn Cu: \(n_{Cu\left(NO_3\right)_2\left(X\right)}=a+0,02\left(mol\right)\)
Bảo toàn \(NO_3^-\): \(n_{AgNO_3\left(X\right)}+2.n_{Cu\left(NO_3\right)_2\left(X\right)}=3.n_{Al\left(NO_3\right)_3\left(B\right)}+2.n_{Cu\left(NO_3\right)_2\left(B\right)}\)
=> \(b+2a+0,04=3.0,027+2.0,02\)
=> 2a + b = 0,081 (2)
(1)(2) => a = 0,018 (mol); b = 0,045 (mol)
=> \(\left\{{}\begin{matrix}n_{AgNO_3\left(X\right)}=0,045\left(mol\right)\\n_{Cu\left(NO_3\right)_2\left(X\right)}=0,038\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(AgNO_3\right)}=\dfrac{0,045}{0,2}=0,225M\\C_{M\left(Cu\left(NO_3\right)_2\right)}=\dfrac{0,038}{0,2}=0,19M\end{matrix}\right.\)

\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(n_{Al}=\dfrac{0,81}{27}=0,03mol\)
\(B:8,12g\left\{{}\begin{matrix}Cu:a\left(mol\right)\\Ag:b\left(mol\right)\\Fe:c\left(mol\right)\end{matrix}\right.\Rightarrow64a+108b+56c=8,12\)(*)
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,03 0,03
\(\Rightarrow c=n_{Fe}=0,03mol\)
Thay vào (*) ta được: \(64a+108b=8,12-0,03\cdot56\left(1\right)\)
\(n_{Fepư}=0,05-0,03=0,02mol\)
\(BTe:2n_{Cu}+n_{Ag}=3n_{Fepư}+2n_{H_2}\)
\(\Rightarrow2a+b=2\cdot0,02+3\cdot0,03\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,03\end{matrix}\right.\)
\(C_{M_{Cu\left(NO_3\right)_2}}=\dfrac{0,05}{0,1}=0,5M\)
\(C_{M_{AgNO_3}}=\dfrac{0,03}{0,1}=0,3M\)

Nung hỗn hợp BaCO3, Cu, FeO chỉ có BaCO3 bị nhiệt phân hủy
BaCO3 → t ∘ BaO + CO2↑ (B)
Rắn A gồm: Cu, FeO, BaO, có thể có BaCO3 dư
Khí B là CO2
CO2 + KOH → KHCO3
CO2 + 2KOH → K2CO3 + H2O
Dung dịch C gồm KHCO3 và K2CO3
KHCO3 + NaOH → K2CO3 + Na2CO3 + H2O
K2CO3 + CaCl2 → CaCO3↓ + 2KCl
A + H2O dư có phản ứng xảy ra:
BaO + H2O → Ba(OH)2
Vây dd D là Ba(OH)2
rắn E là Cu, FeO, có thể có BaCO3 dư
E + HCl dư → khí B + dd F + rắn G
BaCO3 + 2HCl → BaCl2 + CO2↑ + H2O
FeO + 2HCl → FeCl2 + H2O
Dd F gồm: BaCl2, FeCl2 và HCl dư
Rắn G là Cu
A + H2SO4 đặc => hỗn hợp khí H ( từ đây khẳng định chắc chắn A có BaCO3 dư)
BaCO3 + H2SO4 đặc → t ∘ BaSO4↓ + CO2 + H2O
Cu + 2H2SO4 đặc → t ∘ CuSO4 + SO2↑ + 2H2O
2FeO + 4H2SO4 đặc → t ∘ Fe2(SO4)3 + SO2 + 4H2O
Hỗn hợp khí H gồm: SO2 và CO2
Dung dịch I gồm: CuSO4, Fe2(SO4)3, H2SO4 đặc, nóng dư
Kết tủa K là: BaSO4.

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
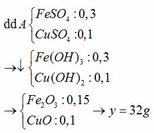

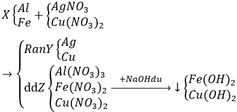
Pt:
Al + 3AgNO3 → Al(NO3)3 + 3Ag↓
2Al + 3Cu(NO3)2 → 2Al(NO3)2 + 3Cu↓
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Al(NO3)3 + 3NaOH → Al(OH)3↓ + 3NaNO3
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Fe(NO3)2 + 2NaOH → Fe(OH)2↓ + 2NaNO3
Cu(NO3)2 + 2NaOH → Cu(OH)2↓ + 2NaNO3


