Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Rồi lọc kết tủa thu được 0,28 gam oxit ?!! ghi đề thiếu -_- Hẳn là nung kết tủa trong không khí ở nhiệt độ cao mới thu được oxit.
Sửa đề: Rồi lọc kết tủa nung trong không khí giàu Oxi ở nhiệt độ cao thi được 0,28 gam oxit ( H=100%)
Cho 16,2g hỗn hợp MgO, Al2O3, MO tác dụng với H2 ở nhiệt độ cao thì:
\(MO\left(0,04\right)+H_2-t^o->M+H_2O\left(0,04\right)\)\(\left(1\right)\)
\(m_{H_2SO_4}\left(bđ\right)=\dfrac{90.15,3}{100}=13,77\left(g\right)\)
Khi dẫn hơi nước qua ống đựng dung dịch H2SO4 trên thì:
\(m_{ddH_2SO_4}\left(sau\right)=\dfrac{13,77.100}{86,34}=15,95\left(g\right)\)
\(\Rightarrow m_{H_2O}\left(thêm-vao\right)=15,95-15,3=0,65\left(g\right)\)
\(\Rightarrow m_{H_2O}\left(bđ\right)=\dfrac{0,65.100}{90}=0,72\left(g\right)\)
\(\Rightarrow n_{H_2O}=0,04\left(mol\right)\)
Khi cho qua HCl, chất rắn M còn lại là 2,56 gam
\(\Rightarrow M_M=\dfrac{2,56}{0,05}=64\)\((g/mol)\)
\(b)\)
Ta có hiệu suất pứ khử bởi H2 chỉ đạt 80%
\(\Rightarrow n_{CuO}=\dfrac{0,04.100}{80}=0,05\left(mol\right)\)
Khi cho chất rắn còn lại trog ống td với dd HCl dư
\(MgO\left(a\right)+2HCl--->MgCl_2\left(a\right)+H_2\)\(\left(2\right)\)
\(Al_2O_3\left(b\right)+6HCl--->2AlCl_3\left(2b\right)+3H_2O\)\(\left(3\right)\)
Gọi a, b lần lượt là số mol của MgO và Al2O3
\(\Rightarrow40a+102b+0,05.80=16,2\)
\(\Rightarrow40a+102b=12,2\left(I\right)\)
Dung dịch B: \(\left\{{}\begin{matrix}MgCl_2:a\left(mol\right)\\AlCl_3:2b\left(mol\right)\\HCl\left(dư\right)\end{matrix}\right.\)
Khi lấy 1/10 dung dịch B trên tác dụng với NaOH dư thì:
\(HCl+NaOH--->NaCl+H_2O\)\(\left(4\right)\)
\(MgCl_2\left(\dfrac{a}{10}\right)+2NaOH--->Mg\left(OH\right)_2\left(\dfrac{a}{10}\right)+2NaCl\)\(\left(5\right)\)
\(AlCl_3+3NaOH--->Al\left(OH\right)_3+3NaCl\)\(\left(6\right)\)
\(Al\left(OH\right)_3+NaOH--->NaAlO_2+2H_2O\)\(\left(7\right)\)
Kết tủa thu được \(Mg\left(OH\right)_2:\dfrac{a}{10}\left(mol\right)\)
\(Mg\left(OH\right)_2\left(\dfrac{a}{10}\right)-t^o->MgO\left(\dfrac{a}{10}\right)+H_2O\)
Oxit thu được là MgO
\(n_{MgO}=\dfrac{0,28}{40}=0,007\left(mol\right)\)
\(\Rightarrow\dfrac{a}{10}=0,007\)
\(\Rightarrow a=0,07\left(II\right)\)
\(\%m_{MgO}=\dfrac{0,07.40.100}{16,2}=17,28\)
\(\%m_{CuO}=\dfrac{0,05.80.100}{16,2}=24,69\%\)
\(\Rightarrow\%m_{Al_2O_3}=58,03\%\)

2 ancol đơn chức chứ bạn đáp án toàn ancol đơn chức =))
nCO2=0,4 mol nH2O=0,4 mol=>nCO2=nH2O
=>hh gồm các ete no đơn chức
Gọi CTTQ ete là CnH2nO
Bảo toàn klg=>mO2=0,4.44+7,2-7,2=17,6g=>nO2=0,55 mol
Bảo toàn O=>nete=nO trg ete=0,4.2+0,4-0,55.2=0,1 mol
=>Mete=72 g/mol
=>CTPT ete là C4H8O
Chỉ có 1 ctct tm CH2=CH-CH2-O-CH3
=>ete này đc tạo bởi 2 ancol CH3OH và CH2=CH-CH2OH
=>chọn D
Ete + O2 \(\rightarrow\)CO2 + Hoh
số mol ete là x
nCO2 = nhoh = 0.4 \(\rightarrow\) m = \(0,4.\left(18+44\right)=24,8\)
Dựa vào bảo toàn khối lượng: mO2 = 24,8 -7.2 = 17,6\(\rightarrow\) nO2 = 0,55
Bảo toàn nguyên tố oxi: x + 0,55 .2 = 0,4.3\(\rightarrow\) x = 0.1
Mete = 7,2/ 0.1 =72\(\rightarrow\) CH3 - O - C3H5
Đáp án D

Ở 100°C là nhiệt độ cao bắt buộc ra KClO3
nCl2=0,6 mol
nKCl=0,5 mol
3Cl2 +6KOH =>5KCl + KClO3 +3H2O
0,6 mol
0,3 mol <=0,6 mol 0,5 mol
Dư 0,3 mol
CM dd KOH=0,6/2,5=0,24M
=>Chon A!!!!

Gọi a,b,c,d lần lượt là số mol của Al,Mg,Fe,Zn
Số mol H2 thu được n = = 0,065
Phương trình phản ứng khi cho hỗn hợp tác dụng với axit
Al Al3+ + 3e
a mol 3a mol
Mg Mg2+ + 2e
b mol 2b mol
Fe Fe2+ + 2e
c mol 2c mol
Zn Zn2+ + 2e
d mol 2d mol
2H+ +2e H2
2.0,065 0,065
ta có phương trình :
3a +2b + 2c + 2d =2.0,065 =0,13 (1)
Khi cho hỗn hợp trên tác dụng với clo thu được muối.như vậy khối lượng Clo có trong muối là : mCl2 = m+ 4,97 –m =4,97 gam
Suy ra nCl2 = 0,07 mol
Tuong tự như phương trình phản ứng trên ta có phương trình toán học
3a +3b + 2c + 2d =0,07.2 =0,14 (2)
Lấy (2) – (1) ta có : b=0,01 .suy ra khối lượng Fe = 0,01 . 56 = 0,56 g

MX=6,25.16 =100
X là este đơn chức chỉ chứa C,H,O nên ta tìm được công thức phân tử là C5H8O2
Xét pư thủy phân 0,2mol X trong 0,3mol KOH
Vì X đơn chức nên pư xảy ra với tỷ lệ 1:1 suy ra KOH dư
Bảo toàn khối lượng ta có mX+mKOH=mrắn khan+mchất bay hơi Y
Suy ra mchất bay hơi Y=20+0,3.56-28=8,8(g)
mà nY=nX=0,2 mol
Vậy MX=8,8/0,2=44 \(\Rightarrow\) X có công thức phân tử C2H4O
Chỉ có đáp án B thỏa mãn

Có 0,1 mol chất béo \(\Rightarrow\) tạo ra 0,1 mol glixerol.
\(\Rightarrow\) m = 0,1 x 92 = 9,2 gam.

\(CuO\left(0,05\right)+CO-t^o->Cu\left(0,05\right)+CO_2\left(0,05\right)\)\(\left(1\right)\)
\(M_xO_y\left(\dfrac{0,04}{y}\right)+yCO-t^o->xM+yCO_2\left(0,04\right)\)\(\left(2\right)\)
Hỗn hợp C:\(\left\{{}\begin{matrix}CO_2\\CO\left(dư\right)\end{matrix}\right.\)
Hỗn hợp chất rắn D:\(\left\{{}\begin{matrix}Cu\\M\end{matrix}\right.\)
Khi Dẫn C vào KOH đặc dư thì chỉ có CO2 tác dụng
\(CO_2+2KOH--->K_2CO_3+H_2O\)\(\left(3\right)\)
Sau phản ứng thấy khối lượng bình tăng thêm 3,96 gam chính là khối lượng CO2 bị hấp thụ vào bình
\(n_{CO_2}=\dfrac{3,96}{44}=0,09\left(mol\right)\)
Khi cho D tác dụng với H2SO4 loãng dư thì thu dduwwocj chất rắn G không tan và đung dịch E sau phản ứng. Chứng tỏ kim loại M tán trong dung dịch H2SO4 loãng dư:
\(2M+nH_2SO_4\left(loang\right)--->M_2\left(SO_4\right)_n+nH_2\)\(\left(4\right)\)
Dung dịch E là: \(M_2\left(SO_4\right)_n\)
Chất rắn G là: \(Cu\)
Khi cho G tác dụng với lượng vừa đủ AgNO3 thì:
\(Cu+2AgNO_3--->Cu\left(NO_3\right)_2+2Ag\)\(\left(5\right)\)
\(n _{Ag}=\dfrac{10,8}{108}=0,1\left(mol\right)\)
Theo (5) \(n_{Cu}=0,05\left(mol\right)\)
Theo (1) \(n_{CuO}=0,05\left(mol\right)\)
\(\Rightarrow m_{CuO}=4\left(g\right)\)
\(\Rightarrow m_{M_xO_y}=6,32-4=2,32\left(g\right)\)
Theo (1) \(n_{CO_2}\left(1\right)=0,05\left(mol\right)\)
\(\Rightarrow n_{CO_2}\left(2\right)=0,04\left(mol\right)\)
\(\Rightarrow n_{M_xO_y}=\dfrac{0,04}{y}\left(mol\right)\)
Ta có: \(\dfrac{0,04}{y}=\dfrac{2,32}{Mx+16y}\)
\(\Leftrightarrow M=\dfrac{1,68y}{0,04x}\)
| \(x\) | \(1\) | \(2\) | \(2\) | \(3\) |
| \(y\) | \(1\) | \(1\) | \(3\) | \(4\) |
| \(M\) | \(42\) \((loại)\) | \(21\)\((loại)\) | \(63\)\((loại)\) | \(56\)\((Fe)\) |
\(\Rightarrow CT:Fe_3O_4\)
\(\%m_{Cu}=63,29\%\)
\(\%m_{Fe_3O_4}=36,71\%\)
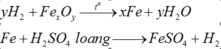
Đáp án A
Fe.