Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
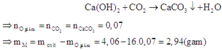
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
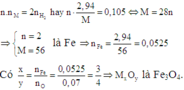
Đáp án D.

Các phương trình xảy ra
RCOOR1 + NaOH → RCOONa + R1OH
Làm bay hơi dung dịch sau thủy phân,sau đó cho qua CaCl2 để hút hết nước,sau đó cho qua K thì có khí nên có phản ứng:
R1OH + K → ROK + 1/2H2
Cho H2 qua CuO
CuO + H2 → Cu + H2O
nCu = 0,1 mol → nH2 = 0,1 mol → nR1OK = 0,2 mol→ MR1OK = (6,2 + mH2)/0,2 = 6,4/0,2 = 32
→ R1OH là CH3OH
Ta có neste = 0,2(mol), nBr2 = 0,2(mol)
→ Este có 1 liên kết đôi ở ngoài mạch C
→ Este có M là 86
→ Đáp án D

Đáp án D
Các phương trình xảy ra
![]()
Làm bay hơi dung dịch sau thủy phân,sau đó cho qua CaCl2 để hút hết nước,sau đó cho qua K thì có khí nên có pứ
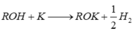
Cho H2 qua CuO

Ta có neste=0,2(mol)
=) Este có 1 liên kết đôi ở ngoài mạch C
=)Este có M là 86

Đáp án D
Bình CaCl2 giữ lại nước. Còn lại là ancol
Khí Z bay ra là H2: ROH + K → ROK + ½ H2
Và H2 + CuO (to) → Cu + H2O
→ n(Cu) = n(H2) = 0,1 mol
→ n(ROH) = 0,2 mol = n(este)
Vậy m(bình K tăng) = m(ancol) – m(H2) → R = 15 → ancol CH3OH
Có: n(Br2) = 0,2 mol = n(este) → chỉ có 1π trong gốc hiđrocacbon của axit.
→ Este sau khi phản ứng với Br2 có dạng: Br2R’COOCH3
có %m(Br) = 65,04% → R’ = 27 (CH2=CH-)
Este là CH2=CHCOOCH3

Đáp án D
nFe = 0,105 => nFe3O4 = 0,035 => m = 0,035.232 = 8,12 => Chọn D.

Đáp án D
nFe = 0,105 => nFe3O4 = 0,035 => m = 0,035.232 = 8,12 => Chọn D.