Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(n_{NaOH}=0,1.1,75=0,175mol\)
\(\Rightarrow\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,175}{0,1}=1,75\)
Ta có: \(1< 1,75< 2\) \(\Rightarrow\) xảy ra 2 pư tạo 2 muối và cả 2 chất đều hết
PTHH: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
\(CO_2+NaOH\rightarrow NaHCO_3\)
Gọi a,b lần lượt là số mol của Na2CO3; NaHCO3
Ta có 2 pt: \(\left\{{}\begin{matrix}a+b=0,1\\2a+b=0,175\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}a=0,075\\b=0,025\end{matrix}\right.\)
\(\Rightarrow m_{Na_2CO_3}=0,075.106=7,95g\)
\(m_{NaHCO_3}=0,025.84=2,1g\)

a) \(n_{CH_3COOH}=0,1.0,3=0,03\left(mol\right)\)
PTHH: CH3COOH + NaOH --> CH3COONa + H2O
0,03---->0,03--------->0,03
=> \(V_{dd.NaOH}=\dfrac{0,03}{1,5}=0,02\left(l\right)\)
b) mCH3COONa = 0,03.82 = 2,46 (g)
c) \(C_{M\left(CH_3COONa\right)}=\dfrac{0,03}{0,1+0,02}=0,25M\)

Ta có: \(\left\{{}\begin{matrix}n_{NaOH}=0,2\cdot0,5=0,1\left(mol\right)\\n_{H_2SO_4}=0,3\cdot1,5=0,45\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,45}{1}\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{Na_2SO_4}=0,05\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{Na_2SO_4}}=\dfrac{0,05}{0,2+0,3}=0,1\left(M\right)\\C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,4}{0,5}=0,8\left(M\right)\end{matrix}\right.\)
200ml = 0,2l
300ml = 0,3l
Số mol của dung dịch natri hidroxit
CMNaOH = \(\dfrac{n}{V}\Rightarrow n=C_M.V=0,5.0,2=0,1\left(mol\right)\)
Số mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}\Rightarrow n=C_M.V=1,5.0,3=0,45\left(mol\right)\)
Pt : 2NaOH + H2SO4 → Na2SO4 + 2H2O\(|\)
2 1 1 2
0,1 0,45 0,05
a) Lập tỉ số so sánh : \(\dfrac{0,1}{2}< \dfrac{0,45}{1}\)
⇒ NaOH phản ứng hết , H2SO4 dư
⇒ Tính toán dựa vào số mol của NaOH
Số mol dư của dung dịch axit sunfuric
ndư= nban đầu - nmol
= 0,45 - \(\left(\dfrac{0,1.1}{2}\right)\)
= 0,4 (mol)
Khối lượng dư của dung dịch xxit sunfuric
mdư = ndư . MH2SO4
= 0,4. 98
= 39,2 (g)
b) Số mol của natri sunfat
nNa2SO4= \(\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
Thể tích của dung dịch sau phản ứng
Vdung dịch sau phản ứng= 0,2 + 0,3
= 0,5 (l)
Nồng độ mol của natri sunfat
CMNa2SO4 = \(\dfrac{n}{V}=\dfrac{0,05}{0,5}=0,1\left(M\right)\)
Nồng độ mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
Chúc bạn học tốt

nNaOH = 0,1 mol
nH2SO4 = 0,1 mol
PT: 2NaOH + H2SO4 -> Na2SO4 + H2O
=> H2SO4 dư: 0,1 - 0,05= 0,05 (mol)
=> mH2SO4 dư = n. M = 0,05 . 98 = 4,9 g
a,\(2NaOH+H2SO4->Na2SO4+2H2O\)
b,theo pthh
PTHH:\(2NaOH+H2SO4->Na2SO4+2H2O\)
theo pthh:\(2\)..................1...........(mol)
theo bài: \(\dfrac{100}{1000}\)............\(\dfrac{9,8}{98}........\)(mol)
\(=>\dfrac{0,1}{2}< \dfrac{0,1}{1}\)=>H2SO4 dư
c,theo pthh \(=>nNA2SO4=\dfrac{1}{2}nNaOH=0,05mol\)
\(=>mNa2SO4=142.0,05=7,1g\)

\(n_{CaCO_3}=\dfrac{45}{100}=0,45\left(mol\right)\\ n_{NaOH}=0,5.1,5=0,75\left(mol\right)\\ CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\\ n_{CO_2}=n_{CaCO_3}=0,45\left(mol\right)\\ Vì:1< \dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,75}{0,45}=\dfrac{5}{3}< 2\\ \Rightarrow Sp:Na_2CO_3,NaHCO_3\\ Đặt:n_{Na_2CO_3}=a\left(mol\right);n_{NaHCO_3}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}2a+b=0,75\\a+b=0,45\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,15\end{matrix}\right.\\ \Rightarrow ddX:m_{Na_2CO_3}=0,3.106=31,8\left(g\right);m_{NaHCO_3}=84.0,15=12,6\left(g\right)\)

\(n_{CO_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
\(m_{NaOH}=\dfrac{200.9}{100}=18\left(g\right)=>n_{NaOH}=\dfrac{18}{40}=0,45\left(mol\right)\)
PTHH: 2NaOH + CO2 --> Na2CO3 + H2O
Xét tỉ lệ: \(\dfrac{0,45}{2}< \dfrac{0,35}{1}\) => NaOH hết, CO2 dư
PTHH: 2NaOH + CO2 --> Na2CO3 + H2O
_______0,45--->0,225----->0,225____________(mol)
Na2CO3 + CO2 + H2O --> 2NaHCO3
0,125<----0,125--------------->0,25____________(mol)
=> \(\left\{{}\begin{matrix}n_{Na_2CO_3}=0,1\left(mol\right)\\n_{NaHCO_3}=0,25\left(mol\right)\end{matrix}\right.=>\left\{{}\begin{matrix}m_{Na_2CO_3}=0,1.106=10,6\left(g\right)\\m_{NaHCO_3}=0,25.84=21\left(g\right)\end{matrix}\right.\)
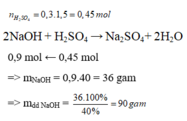
Ta có: \(n_{NaOH}=0,1\cdot1,5=0,15\left(mol\right)\) \(\Rightarrow m_{NaOH}=0,15\cdot40=6\left(g\right)\)