Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(N_2+3H_2\underrightarrow{t^o}2NH_3\)
Ta có: \(K_C=\dfrac{\left[NH_3\right]^2}{\left[N_2\right]\left[H_2\right]^3}=\dfrac{0,6^2}{0,02.2^3}=2,25\)
Theo PT: \(\left[N_2\right]_{\left(pư\right)}=\dfrac{1}{2}\left[NH_3\right]=0,3\left(mol\right)\)
\(\Rightarrow H=\dfrac{0,3}{0,3+0,02}.100\%=93,75\%\)

`1>{1,2}/3->H` tính theo `H_2.`
Tại TTCB: `[H_2]=3/{2}[NH_3]=0,3M`
`->C_{H_2\ pu}=1,2-0,3=0,9M`
`->H={0,9}/{1,2}.100\%=75\%`
Không có đáp án đúng.

a)Tại tđ cân bằng:
\(\left[N_2\right]=0,5-\dfrac{1}{2}.0,1=0,5-0,05=0,45\left(M\right)\)
\(\left[H_2\right]=0,6-\dfrac{3}{2}.0,1=0,6-0,15=0,45\left(M\right)\)
\(\Rightarrow k_c=\dfrac{\left[NH_3\right]^2}{\left[N_2\right].\left[H_2\right]^3}=\dfrac{0,1^2}{0,45.0,45^3}\approx0,244\)
b) Để tăng H tổng hợp \(NH_3\), chúng ta có thể:
- Tăng P bằng cách giảm V (chọn P phù hợp)
- Giảm nhiệt độ của hệ ( chọn nhiệt độ phù hợp)
- Thêm \(N_2;H_2\)

`N_2(g)+3H_2` $\leftrightharpoons$ `2NH_3(g)`
`K_C={[NH_3]^2}/{[N_2].[H_2]^3}={0,3^2}/{0,5.0,1^3}=180`
Không đáp án đúng.

N 2 (k) + 3 H 2 (k) ↔ 2 N H 3 (k)
ΔH = -92 kJ
1. Khi tăng áp suất chung, cân bằng chuyển dịch theo chiều từ trái sang phải là chiều tạo ra số mol khí ít hơn.
2. Khi giảm nhiệt độ, cân bằng chuyển dịch theo chiéu từ trái sang phải là chiều của phản ứng toả nhiệt.
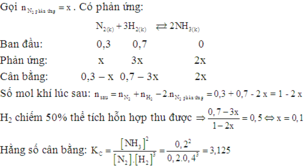

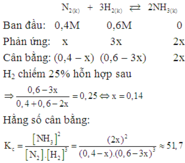

N2+3H2\(\rightarrow\)2NH3
Kcb=\(\dfrac{\left[NH_3\right]^2}{\left[N_2\right].\left[H_2\right]^3}=\dfrac{0,6^2}{0,02.2^3}=2,25\)
Đáp án B