Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi đun nóng :
1g Mg ................................................2,96g Cl
Vậy
24g Mg ....................................................71g Cl
nMg=24/24=1(mol)
nCl=71/35,5=2(mol)
Vậy công thức hoá học của hợp chất là

Khi đun nóng :
1g Mg ................................................2,96g Cl
Vậy
24g Mg ....................................................71g Cl
\(n_{Mg}=\dfrac{24}{24}=1\left(mol\right)\)
\(n_{Cl}=\dfrac{71}{35,5}=2\left(mol\right)\)
Vậy công thức hoá học của hợp chất là \(MgCl_2\)

Giả sử hợp chất có khối lượng 7g → m M g = 3g ; m S = 4g
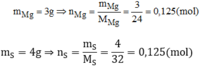
Vậy trong hợp chất: 0,125 mol nguyên tử Mg và 0,125 mol nguyên tử S. Có nghĩa là 1 mol nguyên tử Mg kết hợp với 1 mol nguyên tử S.
Nên công thức hóa học đơn giản của magie sunfua: MgS.

a) Mg + Cl2 --to--> MgCl2
Tỉ lệ Mg : Cl2 = 1:1
b) Theo ĐLBTKL:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\)
=> \(m_{Cl_2}=19-4,8=14,2\left(g\right)\)
=> \(n_{Cl_2}=\dfrac{14,2}{71}=0,2\left(mol\right)\)
=> \(V_{Cl_2}=0,2.22,4=4,48\left(l\right)\)
c) \(n_{MgCl_2}=\dfrac{3.10^{23}}{6.10^{23}}=0,5\left(mol\right)\)
PTHH: Mg + Cl2 --to--> MgCl2
______0,5<--0,5<--------0,5__________(mol)
=> Số nguyên tử Mg = 0,5.6.1023 = 3.1023
=> Số phân tử Cl2 = 0,5.6.1023 = 3.1023

a) CTTQ MgxSy (x,y: nguyên, dương)
Ta có: mMg/ mS= 3/4
<=> 24x/32y=3/4
<=>x/y=1/1
=> CTHH đơn giản: MgS
b) nMg= 1/3 (mol)
nS= 0,25(mol)
PTHH: Mg + S -to-> MgS
Ta có: 1/3 : 1 > 0,25/1
=> Mg dư, S hết, tính theo nS
=> nMgS=0,25(mol) -> mMgS= 56.0,25=14(g)
mMg(dư)= 8 - 0,25.24=2(g)
=> Chọn D

Bài 2:
1. Cl2
\(PTK_{Cl_2}=2.NTK_{Cl}=2.35,5=71\left(đ.v.C\right)\)
2. Mg(OH)2
\(PTK_{Mg\left(OH\right)_2}=NTK_{Mg}+2.\left(NTK_O+NTK_H\right)\\ =24+2.\left(16+1\right)=58\left(đ.v.C\right)\)
3. ZnCl2 (2Cl mới đúng)
\(PTK_{ZnCl_2}=NTK_{Zn}+2.NTK_{Cl}=65+2.35,5=136\left(đ.v.C\right)\)
4. Cu
NTKCu= 64(đ.v.C)
5. Al2O3
\(PTK_{Al_2O_3}=2.NTK_{Al}+3.NTK_O=2.27+3.16=102\left(đ.v.C\right)\)
6. NH3
\(PTK_{NH_3}=NTK_N+3.NTK_H=14+3.1=17\left(đ.v.C\right)\)
7. Ag
NTKAg=108(đ.v.C)
8. H2SO4
\(PTK_{H_2SO_4}=2.NTK_H+NTK_S+4.NTK_O\\ =2.1+32+4.16=98\left(đ.v.C\right)\)
1.Cl2 (71)
2. Mg(OH)2 (58)
3. ZnCl2 (136)
4. Cu (64)
5. Al2O3 (102)
6. NH3 (17)
7. Ag (108)
8. H2SO4 (98)

a) N2, NaCl, Fe2O3, Mg, CaCO3
b)
Đơn chất: N2, Mg
Hợp chất: NaCl, Fe2O3, CaCO3
nMg=m/M= 1/24 (mol)
nCl2= m/M=2.96/71 (mol)
Gọi: CT của muối : MgClx
2Mg + xCl2 -to-> 2MgClx
2_______x
1/24_____2.96/71
<=> 1/24*x = 2.96/71*2
=> x = 2
Vậy: CT của muối : MgCl2
Công thức tính bài này là j vậy bạn