Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
A có công thức CnH2n-2O2 ( n≥ 3), và B có công thức CmH2mO2 ( m≥2)
Vì dung dịch Ca(OH)2 dư nên nCO2 = nCaCO3 = 0,4 mol
mbình tăng = mCO2 + mH2O → nH2O = 0,35 mol
Luôn có nA = nCO2 - nH2O = 0,05 mol → nB = 0,15 -0,05 = 0,1 mol
→ 0,05n + 0,1m = 0,4 → n + 2m = 8
Vậy chỉ có cặp nghiệm nguyên thỏa mãn là n = 4 và m= 2
Công thức của 2 este là C2H4O2, C4H6O2

ĐÁP ÁN: A
X gồm C3H8; C2H6O2; ancol khác.
Vì số mol C3H8 và C2H6O2 bằng nhau ⇒ qui về C3H8O và C2H6O
⇒ Hỗn hợp X gồm các ancol no đơn chức mạch hởbình tăng
Bảo toàn khối lượng:
Ta có:
Bảo toàn O:

Quy đổi: CnH4 => 12n+4 = 34 => n trung bình là 2,5
Áp dụng bảo toàn nguyên tố:nCO2 = 2,5 . 0,05 = 0,125 mol
nH2O = 0,2 mol
=> m = 0,125.44 + 0,1.18 = 7,3 g.
mol H2O phải =0,1mol vì bảo toàn ng tố H+ theo mol CnH4 .Việt viết nhầm thôi chứ thay vào đ/a đúng mà,,

nCu(OH)2=0,08 mol
2C3H5(OH)3 + Cu(OH)2 => [C3H5(OH)2O]2Cu + 2H2O
0,16 mol<=0,08 mol
C3H8O3 +7/2 O2 =>3CO2 +4H2O
0,16 mol=>0,56 mol
nO trong C3H8O3=0,16.3=0,48 mol
Mà tổng nO2=37,408/22,4=1,67 mol
=>nO2 đốt cháy ancol=1,11 mol
CnH2n+1OH+3n/2 O2 =>nCO2 + (n+1)H2O
=>n ancol no đơn=1,11/1,5n mol
=>nO trong ancol no đơn=1,11/1,5n mol=0,74/n mol
=>tổng nO trong hh ancol=0,48+0,74/n mol
=>mO=7,68+11,84/n gam
m hh ancol=0,74/n (14n+18)+0,16.92
=10,36+13,32/n+14,72=25,08+13,32/n gam
=>%mO=39,785% =(7,68+11,84/n)/(25,08+13,32/n)
=>n=2,84623
Thay vào ct tính số mol co nhh ancol no đơn=0,74/2,846=0,26 mol
Mtb của hh ancol no đơn=12.2,846+2.2,846+18=57,844
=>mhh ancol no đơn=57,844.0,26=15,04 gam
=>%mC3H8O3=0,16.92/(0,16.92+15,04).100%=49,46% chọn C

Ta gọi nC=x ;nH=y ta được 12x+y=4,64
Ta có: m dd giảm=mkếttủa - (mCO2 + mH2O) => mCO2+mH2O
=mkettua- mdd giảm=39,4-19,912=19,488g
=> 44x+18.0,5y=10,688
Giải hpt: x=0,348; y=0,464 => x:y=3:4
=> CTĐGN của X là C3H4 => CTPT là C3H4.
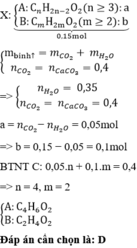

Ta có khối lượng bình tăng chính là tổng khối lượng của CO2 và H2O:
Gọi n và m lần lượt là số cacbon của este no và không no.
Ta có: